1、选择题 下列溶液中各微粒的浓度关系不正确的是(? )
A.0.1 mol・L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.1 L 0.l mol・L-1CuSO4・(NH4)2SO4・6H2O溶液中:
c(SO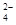 )>c(NH
)>c(NH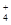 )>c(Cu2+)>c(H+)>c(OH-)
)>c(Cu2+)>c(H+)>c(OH-)
C.等体积、等物质的量浓度的醋酸和醋酸钠混合后的溶液中:
c(CH3COO-)>c(Na+) >c(H+)>c(OH-)
D.0.1 mol・L-1NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)=c(CO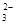 )+c(OH-)
)+c(OH-)
参考答案:D
本题解析:A 正确,符合电荷守恒
B 正确,氨根离子、硫酸根离子物质的量相等,但由于氨根离子水解,使氨根离子浓度小于硫酸根离子浓度,先考虑溶质,再考虑水电离出的c(H+)、c(OH-),由于氨根离子、铜离子水解,溶液显酸性,c(H+)>c(OH-)
C 正确,溶液显酸性,c(H+)>c(OH-),根据电荷守恒,c(CH3COO-)>c(Na+)
D 错误,c(Na+)+c(H+) =2c(CO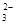 )+c(OH-)+ c(HCO3-)
)+c(OH-)+ c(HCO3-)
本题难度:一般
2、填空题 有盐AmBn的溶液。(1)若为强酸弱碱盐,是水解的离子方程式是:?。(2)若为弱酸强碱盐,是水解的离子方程式是:?。
参考答案:①An++nH2O A(OH)n+nH+;②Bm-+H2O
A(OH)n+nH+;②Bm-+H2O HB(m-1)-+OH-。
HB(m-1)-+OH-。
本题解析:若为强酸弱碱盐,弱碱的阳离子的水解的离子方程式一步写出,即An++nH2O A(OH)n+nH+;若为弱酸强碱盐,弱酸的阴离子的水解的离子方程式要分步来写,但一般以第一步为主,后面由于太弱可省略,即Bm-+H2O
A(OH)n+nH+;若为弱酸强碱盐,弱酸的阴离子的水解的离子方程式要分步来写,但一般以第一步为主,后面由于太弱可省略,即Bm-+H2O HB(m-1)-+OH-。
HB(m-1)-+OH-。
本题难度:一般
3、实验题 硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。某研究小组设计SnSO4制备路线如下:
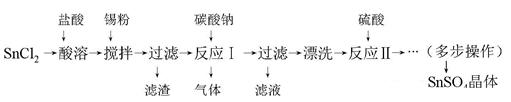
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因?。
(2)加入Sn粉的作用有两个:①调节溶液pH?②?。
(3)反应Ⅰ生成的气体为CO2,得到的沉淀是SnO。该沉淀经过滤后需漂洗,如何证明沉淀已经洗涤完全? ?。
(4)多步操作包含的具体实验步骤的名称可以是:?。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是?。
(6)该小组通过下列方法测所用锡粉样品的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl→SnCl2 + H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:6FeCl2 + K2Cr2O7 + 14HCl →6FeCl3 + 2KCl + 2CrCl3 +7H2O
取1. 226 g 锡粉样品,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液32.00 mL。则该锡粉样品中锡的质量分数是?
参考答案:(1)加入盐酸,使水解平衡向左移动,抑制Sn2+水解
(2)防止Sn2+被氧化
(3)取最后一次洗涤液,向其中加入AgNO3溶液,若无沉淀,则说明已洗涤干净
(4)加热浓缩、冷却结晶、过滤、洗涤
(5)Sn2+ + H2O2 +2H+=Sn4+ +2H2O
(6)93.18%
本题解析:(1)SnCl2在水中发生水解反应:SnCl2+H2O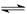 Sn(OH)Cl+HCl. 生成难溶物Sn(OH)Cl,使溶液变浑浊。若加入HCl,可使平衡向逆反应方向移动,抑制Sn2+水解。
Sn(OH)Cl+HCl. 生成难溶物Sn(OH)Cl,使溶液变浑浊。若加入HCl,可使平衡向逆反应方向移动,抑制Sn2+水解。
(2)由于在酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。为了调节调节溶液pH并防止Sn2+被氧化为Sn4+要加入Sn粉。
(3)在反应过程中加入了HCl,沉淀的表面会有Cl-存在,只要能证明在洗涤液中无Cl-存在就可以证明沉淀已经洗涤完全。具体的检验方法是取最后一次洗涤液,向其中加入AgNO3溶液,若无沉淀,则说明已洗涤干净。
(4)在多步操作中所包含的具体实验步骤的名称是加热浓缩、冷却结晶、过滤、洗涤。
(5)酸性条件下,SnSO4与双氧水发生反应的离子方程式是Sn2+ + H2O2 +2H+=Sn4+ +2H2O。
(6)在处理过程中发生的反应为:Sn + 2HCl=SnCl2 + H2↑;2FeCl3+SnCl2=2FeCl2+ SnCl4
6FeCl2 + K2Cr2O7 + 14HCl =6FeCl3 + 2KCl + 2CrCl3 +7H2O。由方程式得关系式3Sn―3SnCl2 ―6FeCl3 ― K2Cr2O7.因为n(K2Cr2O7)="C・V=0.1000" mol/L×0.032L=3.2×10-3mol.所以n(Sn)= 3×3.2×10-3mol ="9.6" × 10-3mol.m(Sn)=n・M=9。6×10-3mol×119g/mol=1.14g.该锡粉样品中锡的质量分数是(1.14g÷1. 226 g) ×100%=93.18%.4制备、性质反应原理等的知识。
本题难度:一般
4、选择题 下列溶液中各微粒的浓度关系正确的是
A.0.1 mol・L-1 NaHSO4溶液中:[Na+]>[SO42-]>[H+]>[OH-]
B.0.1 mol・L-1Na2S溶液中:2[Na+]=[S2-]+[HS-]+[H2S]
C.0.1 mol・L-1 NaHCO3溶液中:[Na+]+[H+]=[HCO3-]+2[CO32-]+[OH-]
D.等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后:[Na+]=[CH3COO-]>[H+]=[OH-]
参考答案:C
本题解析:A、硫酸氢钠溶于水完全电离出H+、Na+、SO42-,所以0.1 mol・L-1 NaHSO4溶液中离子浓度大小关系是[H+]>[Na+]=[SO42-]>[OH-],A不正确;B、根据物料守恒可知 0.1 mol・L-1Na2S溶液中:[Na+]=2[S2-]+2[HS-]+2[H2S],B不正确;C、根据电荷守恒可知0.1 mol・L-1 NaHCO3溶液中:[Na+]+[H+]=[HCO3-]+2[CO32-]+[OH-],C正确;D、乙酸是弱酸,则 等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后恰好反应生成的乙酸钠水解,溶液显碱性,则溶液中离子浓度大小关系是[Na+]>[CH3COO-]>[OH-]>[H+],D不正确,答案选C。
本题难度:一般
5、选择题 在蒸发皿中加热蒸干并灼烧(低于400℃)下列物质的溶液,可以得到该物质固体的是
A.氯化铝
B.碳酸氢镁
C.碳酸钠
D.高锰酸钾
参考答案:C
本题解析:氯化铝为强酸弱碱盐,水解生成了氢氧化铝,加热灼烧后为氧化铝,故A不能选;B中碳酸氢镁在加热灼烧后,生成了碳酸镁和水和二氧化碳,故B不能选,碳酸钠在在蒸发皿中加热蒸干并灼烧(低于400℃)。得到的还是碳酸钠,故C为本题的答案;高锰酸钾加热会分解为锰酸钾、二氧化锰和氧气,故D不能选。
点评:本题考查了盐类水解、物质的热稳定性,该考点是高考考查的重点和难点,本题难度不大,关键是熟悉各物质的相关性质。
本题难度:简单