1������� ��6��)������ĿҪ����д��ѧ���
(1)̼�����Ƶĵ��뷽��ʽ?��
(2) �ƺ�ˮ��Ӧ�����ӷ���ʽ?��
(3) ����CO2��2OH��===?CO32����H2O�Ļ�ѧ����ʽ?��
�ο��𰸣�(��6��)? (��ѧʽ����û��ƽ�����÷�) (��2�֣���6��)
(1) Na HCO3? =? Na + +H CO3-
(2)2 Na+2 H2O ="2" Na++2OH-+ H2��
(3) CO2 + 2 NaOH = Na2 CO3 + H2O
�����������1��̼���������������ʽ�Σ���������뷽��ʽ��Na HCO3��Na + +H CO3-��
��2���Ƽ���ˮ��Ӧ�����������ƺ���������Ӧ�����ӷ���ʽ��2 Na+2 H2O ="2" Na++2OH-+ H2����
��3���������������ӷ���ʽ��֪���÷���ʽ��ʾ����CO2Ͷ��ǿ����Һ�еķ�Ӧ��������Ӧ��ǿ��������������ơ��������صȣ���Ӧ�Ļ�ѧ������CO2 + 2 NaOH = Na2 CO3 + H2O��
�������ڸ��ݻ�ѧ����ʽ��д���ӷ���ʽʱ���ؼ���ȷ�жϳ���Щ�����û�ѧʽ��ʾ����Щ���������ӷ��ϱ�ʾ��ֻ��ͬʱ�������ܡ�����IJ��ܲ�����ӵ���ʽ�������ȫ���û�ѧʽ��ʾ��
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��ȷ����
[? ]
A��H2SO4��Ba(OH)2��Һ��Ӧ��Ba2+��OH-��H+��SO42-=BaSO4����H2O
B��CuSO4��Һ����H2S���壺Cu2+��H2S=CuS����2H+
C��AlCl3��Һ�м��������Ũ��ˮ��Al3+��4NH3��H2O=AlO2-��4NH4+��2H2O
D�����������Ũ�ȵ�Ba(OH)2ϡ��Һ��NH4HCO3ϡ��Һ��ϣ�
Ba2+��2OH-��NH4+��HCO3-=BaCO3����NH3��H2O��H2O
�ο��𰸣�BD
���������
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�?��
A?ͭ�����ᷴӦ��Cu +2H��??Cu2�� + H2��
B?�������Ȼ�����Һ��Ӧ��Ba2�� + SO42��??BaSO4��
C?��������ˮ��Ӧ��2Na +? 2H��??2Na�� + H2��
D?�Ȼ���������ˮ��Ӧ��Fe2+ + Cl2??Fe3��+2Cl��?
�ο��𰸣�B
����������ڽ����˳�����ͭ������ĺ��棬�����û����е��⣬A����ȷ��C��ˮӦ���û�ѧʽ���ǣ���ȷ����2Na��2H2O=2Na����2OH����H2����D��û����ƽ����ȷ����2Fe2+ + Cl2??2Fe3��+2Cl�������Դ���B��
�����Ѷȣ�һ��
4������� A��B��C��D��E��FΪԭ�������������������Ԫ�أ����г�F���Ϊ����������Ԫ�أ�������A��B��C�ij������ʾ�Ϊ��ɫ����ζ�����壬D��E��F�ĵ��ʾ�Ϊ���壬��F������Ŀǰ������ʹ�������Ľ�����A������Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ�C��Eͬ���壬��E��ԭ������ΪC��2����D�����������������ڲ��1�������û�ѧ����ش��������⣺
��1��C�����ӽṹʾ��ͼΪ______��D��E��Ԫ�ص����Ӱ뾶��D______E�����������������=������
��2����A��̼Ԫ����ɵ�ԭ�Ӹ�����3��1�������Ľṹ��ʽΪ______��
��3��A��C�γɵ�10������������A��E�γɵ�18���������ӷ�Ӧ�����ӷ���ʽΪ______��
��4��B������������ˮ���������⻯�ﷴӦ���ɵ��ε�ˮ��Һ��PH______7�����������������=������������AB3��һ����ɫ��Һ̬���ʣ���ײ����ֽ�����ֵ��ʣ���д���÷�Ӧ�Ļ�ѧ����ʽ______��
��5����֪һ�������£�D������������F3O4��Ӧʱ���ų�����������ʹF�����ۻ�����д���÷�Ӧ�Ļ�ѧ����ʽ______��
��6������Ԫ���е�����Ԫ�ؿ��γ�һ�ָ��Σ��������Ӹ�����Ϊ1��1��2�����������Һ����μ���ŨNaOH��Һʱ���Ȳ�����ɫ��������������ܽ⣻ͬʱ�д̼�����ζ������ų��������������ữ��BaCl2��Һ��Ҳ�а�ɫ������������ø��εĻ�ѧʽΪ______��
�ο��𰸣�������A��B��C�ĵ��ʾ�Ϊ��ɫ����ζ�����壬�������ʾ�Ϊ��ɫ��ζ��������H2��N2��O2��F������Ŀǰ������ʹ�������Ľ�����˵��FΪ����A������Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ�˵��A����Ԫ�أ�C��Eͬ���壬��E��ԭ������ΪC��2������������ֻ������������ԭ������Ϊ8�����ԭ������Ϊ16��D�����������������ڲ��1����A��B��C��D��E��FΪԭ�������������������Ԫ�أ�CΪ����˵��D�ڵ������ڣ���Dԭ�ӵĺ������������Ӳ㣬��һ���Ӳ���2�����ӣ�����㼴������Ӧ��3�����ӣ�����������Ϊ13����Ϊ������AΪH��BΪN��CΪO��DΪAl��EΪS��FΪFe��
��1����ԭ��������Ų�6�����ӣ��õ��������Ӻ��γ�O2-��O2-���ӽṹʾ��ͼΪ
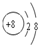
�����뾶��С�ȽϿ����Ӳ��������Ӳ���Խ�࣬�뾶Խ��D������Al3+��E������S2-��Al3+���ӽṹʾ��ͼΪ
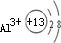
��S2-���ӽṹʾ��ͼΪ
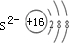
��Al3+����2�����Ӳ㣬S2-����3�����Ӳ㣬�����Ӱ뾶��Al3+��S2-��
�ʴ�Ϊ��
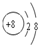
������
��2��A����Ԫ�أ���H��̼Ԫ����ɵ�ԭ�Ӹ�����3��1�Ļ���������ʽΪCH3���ٽ������ͨʽ��CnH2n+2������
��û�����ķ���ʽΪ��CH3��n��n=1������ʽΪCH3������������ͨʽ��n=2������ʽΪC2H6��Ϊ���飬��������ͨʽ��n=3������ʽΪC3H9������������ͨʽ���ʿ�ȷ���û�����Ϊ����C2H6���ṹ��ʽΪCH3-CH3��
�ʴ�Ϊ��CH3-CH3��
��3��H��O�γɵ�10������������OH-��H��S�γɵ�18������������HS-��HS-����ʽ�����ӣ�����OH-��Ӧ����Ӧ�����ӷ���ʽΪHS-+OH-�TS2-+H2O��
�ʴ�Ϊ��HS-+OH-�TS2-+H2O��
��4��B��NԪ�أ���������������ˮ������HNO3�������⻯����NH3��HNO3��NH3��Ӧ���ɵ�����NH4NO3��Ϊǿ�������Σ���������ˮ��ԭ�����⣬ǿ��������ˮ������ԣ�����NH4NO3ˮ��Һ�����ԣ�pH��7��
������AB3��HN3���������⣬��ײ����ֽ�����ֵ��ʣ�ֻ����H2��N2�����ݷ�Ӧ���������д������ʽ����ƽ����2HN3�TH2��+3N2����
�ʴ�Ϊ������2HN3=H2��+3N2����
��5��D������Al����������F3O4��Ӧʱ���ų�����������ʹFe�����ۻ����÷�ӦΪ���ȷ�Ӧ�����ݷ�Ӧ���������д������ʽ����ƽ����8Al+3Fe3O4?����?.?4Al2O3+9Fe��
�ʴ�Ϊ��8Al+3Fe3O4?����?.?4Al2O3+9Fe��
��6������ָ�����������Ӻ�һ�����������ɵ��Σ��������Һ����μ���ŨNaOH��Һʱ���Ȳ�����ɫ��������������ܽ⣬˵������Al3+����ӦΪAl3++3OH-�TAl��OH��3����
Al��OH��3+OH-�TAlO2-+2H2O��ͬʱ�д̼�����ζ������ų���˵������NH4+����ӦΪNH4++OH-�TNH3?H2O�����������ữ��BaCl2��Һ��Ҳ�а�ɫ����������˵�����������SO42-����ӦΪ
SO42-+Ba2+�TBaSO4�����ʸø����к�NH4+��Al3+��SO42-�������������Ӹ�����Ϊ1��1��2����ϻ��ϼ۴����͵����㼴��ȷ���ø��εĻ�ѧʽΪNH4Al��SO4��2��
�ʴ�Ϊ��NH4Al��SO4��2��
���������
�����Ѷȣ�һ��
5������� �ڱ���̼������Һ��ͨ��������CO2����Һ���л��dz��֣�д���÷�Ӧ�����ӷ���ʽ______����������������ԭ���������ͬ�¶��£�NaHCO3�ܽ��С��Na2CO3���⣬��������ԭ����______��______�����Ҫ֤�������γɵĹ����л�����Na2CO3����������Լ���______����Ӧ�����ӷ���ʽΪ______��
�ο��𰸣�̼������CO2��ˮ��Ӧ������ʽ��NaHCO3��NaHCO3�ܽ��С��Na2CO3�����ҷ�Ӧ���ɵ�NaHCO3����������ԭ��Na2CO3�࣬�ܼ��������٣���Һ���л��dz��֣���Ӧ�����ӷ���ʽΪ2Na++CO32-+H2O+CO2=2NaHCO3����Na2CO3��BaCl2��CaCl2��Ӧ����BaCO3��CaCO3����������֤�������γɵĹ����л�����Na2CO3���ɼ���BaCl2��CaCl2��
�ʴ�Ϊ��2Na++CO32-+H2O+CO2=2NaHCO3������Ӧ���ɵ�NaHCO3����������ԭ��Na2CO3�ࣻ?�ܼ��������٣�BaCl2��Ba2++CO32-=BaCO3��������CaCl2��ɣ���
���������
�����Ѷȣ�һ��