1、选择题 一定温度下,在密闭容器中发生反应:A(g)+3B(g)  ?2C(g)达到平衡的标志
?2C(g)达到平衡的标志
A.A、B、C的浓度不再随时间的变化而变化
B.单位时间生成n molA 同时生成3n molB
C.C生成的速率等于A分解的速率的2倍
D.A、B、C的分子数比为1:2:3
参考答案:A
本题解析:可逆反应达到平衡的标志为:1、正、逆反应速率相等;2、体系中各组分的浓度保持不变;
A正确,A、B、C的浓度不再随时间的变化而变化即达平衡;
B错,单位时间生成n molA 同时生成3n molB无论平衡与否均为这样反应;
C错,C生成的速率等于A分解的速率的2倍无论平衡与否均为这样反应;
D错,A、B、C的分子数比为1:2:3不一定达平衡,可能平衡也可能未平衡;
本题难度:一般
2、选择题 800℃时,某反应达到平衡,平衡常数K=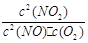 。恒容时,温度降低,NO浓度减小。下列说法正确的是( )
。恒容时,温度降低,NO浓度减小。下列说法正确的是( )
A.该反应是焓变为负值
B.恒温恒容下,通入Ar气以增大压强,则平衡右移
C.升高温度,逆反应速率减小
D.该反应化学方程式为2NO2(g)  2NO(g)+O2(g)
2NO(g)+O2(g)
参考答案:A
本题解析:根据平衡常数的表达式可知,方程式为2NO(g)+O2(g) 2NO2(g),D不正确。温度降低,NO浓度减小,说明平衡向正反应方向进行,即正反应是放热反应,S正确。B不正确,此时物质的浓度不变,平衡不移动。升高温度,反应速率都是增大的,C不正确。答案选A。
2NO2(g),D不正确。温度降低,NO浓度减小,说明平衡向正反应方向进行,即正反应是放热反应,S正确。B不正确,此时物质的浓度不变,平衡不移动。升高温度,反应速率都是增大的,C不正确。答案选A。
本题难度:一般
3、填空题 lmol MnO2粉末加入50mL过氧化氢的溶液里(ρ=1.1g・L-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示
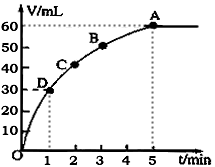
(1)实验时放出气体总体积是__________
(2)放出一半气体所需的时间约为__________
参考答案:(1)60ml
(2)1min
本题解析:
本题难度:一般
4、选择题 下列实验事实不能用平衡移动原理解释的是? ( )。
A.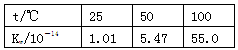
B.
C.
D.
参考答案:D
本题解析:A项,水的电离是可逆过程,升高温度Kw增大,促进水的电离,正确;B项,存在平衡2NO2 N2O4,升高温度平衡向生成NO2方向移动,正确;C项,氨水中存在电离平衡,浓度越稀,电离程度越大,但离子浓度降低,c(OH-)越小,pH越小,正确。D项,对可逆反应2HI(g)?H2(g)+I2(g),增大平衡体系的压强,平衡不移动,故不能用勒夏特列原理解释。但体系中各气体的浓度均增大,颜色变深。
N2O4,升高温度平衡向生成NO2方向移动,正确;C项,氨水中存在电离平衡,浓度越稀,电离程度越大,但离子浓度降低,c(OH-)越小,pH越小,正确。D项,对可逆反应2HI(g)?H2(g)+I2(g),增大平衡体系的压强,平衡不移动,故不能用勒夏特列原理解释。但体系中各气体的浓度均增大,颜色变深。
本题难度:简单
5、填空题 向密闭容器中通入A mol H2和B mol N2,在一定条件下达到平衡,容器中还剩余Cmol N2。
(1)生成NH3的物质的量为____________。
(2)平衡时H2的转化率为____________。
(3)若将容器体积减小一半,则正反应速率变_______;逆反应速率变_______;N2的转化率变______。
参考答案:(1)2(B-C)mol
(2)3(B-C)/A
(3)大;大;大
本题解析:
本题难度:一般