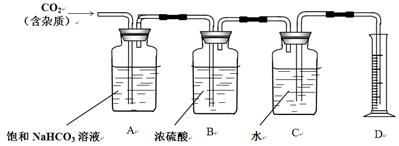
1、实验题 酸性KMnO4溶液能与草酸(H2C2O4)溶液反应。某探究小组利用反应过程中溶液紫色消失快慢的方法来研究影响反应速率的因素。
Ⅰ.实验前首先用浓度为0.1000mol?L-1酸性KMnO4标准溶液滴定未知浓度的草酸。
(1)写出滴定过程中发生反应的化学方程式为??。
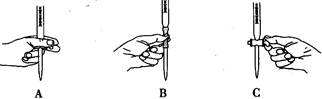
(2)滴定过程中操作滴定管的图示正确的是??。
(3)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度?
(填“偏高”、“偏低”、或“不变”)。
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol・L-1 。用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL)。
实验编号
| 温度(℃)
| 催化剂
用量(g)
| 酸性高锰酸钾溶液
| 实验目的
a. 实验1和2探究?;
b. 实验1和3探究反应物浓度对该反应速率的影响;
c. 实验1和4探究催化剂对该反应速率的影响。
|
体积
(mL)
| 浓度
(mol?L-1)
|
1
| 25
| 0.5
| 4
| 0.1000
|
2
| 50
| 0.5
| 4
| 0.1000
|
3
| 25
| 0.5
| 4
| 0.0100
|
4
| 25
| 0
| 4
| 0.1000
|
?
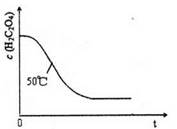
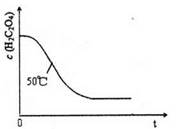
(4)写出表中a 对应的实验目的?;若50°C时,草酸浓度c(H2C2O4)随反应时间t的变化曲线 如下图所示,保持其他条件不变,请在图中画出25°C时c(H2C2O4)随t的变化曲线示意图。
(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
实验编号
| 溶液褪色所需时间(min)
|
第1次
| 第2次
| 第3次
|
1
| 14.0
| 13.0
| 11.0
|
3
| 6.5
| 6.7
| 6.8
|
分析上述数据后得出“当其它条件相同时,酸性高锰酸钾溶液的浓度越小,褪色时间就越短,即反应速率就越快”的结论。甲同学认为该小组“探究反应物浓度对速率影响”的实验方案设计中存在问题,从而得到了错误的实验结论,请简述甲同学改进的实验方案?。
(6)该实验中使用的催化剂应选择MnSO4而不是MnCl2,原因可用离子方程式表示为?。
参考答案:(每空2分)
(1)2MnO4―+5H2C2O4+6H+= 2Mn2+ + 10CO2 ↑+ 8H2O
(2)A
(3) 偏高
(4)探究温度不同对反应速率的影响
(5)其它条件相同时,利用等量且少量的高锰酸钾与等体积不同浓度的足量草酸溶液反应,测量溶液褪色时间。
(6)2MnO4―+ 10Cl― + 16H+ = 5Cl2↑+ 2Mn2+ + 8H2O
本题解析:(1)草酸(H2C2O4)溶液与酸性KMnO4溶液发生氧化还原反应,草酸被氧化为二氧化碳,高锰酸钾被还原为Mn2+,离子方程式为2MnO4―+5H2C2O4+6H+= 2Mn2+ + 10CO2 ↑+ 8H2O;
(2)酸性高锰酸钾氧化性强,所以在该实验中选择酸式滴定管,滴定时用左手的大拇指、食指、中指旋转滴定管的旋塞,所以答案选A;
(3)若滴定前滴定管尖嘴处有气泡,对初读数无影响,但滴定后消失,会使末读数偏大,二者的差值为酸性高锰酸钾溶液滴定的体积,导致计算出的草酸溶液的浓度偏高;
(4)实验1和2相比,只有温度不同,所以a的目的是探究温度不同对反应速率的影响;25°C低于50°C,所以反应速率慢,溶液褪色所需时间长,所画曲线的起点相同,较平缓,在50°C曲线的略上方即可;
(5)探究反应物浓度对速率影响时应在其他条件不变时改变某种反应物的浓度,在本实验中褪色的是酸性高锰酸钾溶液,所以酸性高锰酸钾的溶液的体积、浓度 应是不能变的,而只改变草酸的浓度(体积不变),观察溶液褪色的时间,所以其它条件相同时,利用等量且少量的高锰酸钾与等体积不同浓度的足量草酸溶液反应,测量溶液褪色时间。
(6) 该实验中使用的催化剂应选择MnSO4而不是MnCl2,是因为氯离子与酸性高锰酸钾溶液发生氧化还原反应 而生成氯气,消耗酸性高锰酸钾溶液,使滴定结果偏高,发生的离子方程式是2MnO4―+ 10Cl― + 16H+ = 5Cl2↑+ 2Mn2+ + 8H2O
本题难度:一般
2、选择题 在配制物质的量浓度溶液的实验中,最后用胶头滴管定容后,液面正确的是
A.
B.
C.
D.
参考答案:B
本题解析:考查一定物质的量浓度溶液的配制。定容时液面的最低点与刻度线相切,所以选项B正确,答案选B。
本题难度:简单
3、计算题 下列实验操作正确的是
A.用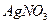 溶液检验两瓶均为红棕色的气体:
溶液检验两瓶均为红棕色的气体: 和
和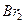 蒸汽
蒸汽
B.用托盘天平称取4.56克食盐
C.苯酚粘到手上,应马上用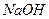 溶液清洗
溶液清洗
D.用量筒量取2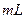 98%的浓
98%的浓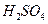 ,向其中加水稀释至8Ml
,向其中加水稀释至8Ml
参考答案:A
本题解析:托盘天平只能精确到0.1克。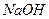 溶液有腐蚀性。量筒不能作稀释用的容器,且水不能加入浓
溶液有腐蚀性。量筒不能作稀释用的容器,且水不能加入浓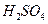 中。选A。
中。选A。
本题难度:简单
4、选择题 下列实验操作中正确的是

A.蒸发操作时,使混合物中的水分完全蒸干后,才停止加热
B.蒸馏操作时,冷凝水应从冷凝管夹层的上口进入
C.进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
参考答案:C
本题解析:略
本题难度:简单
5、填空题 作为高中生,学会利用我们课堂上学到的知识来解决生活中的一些问题,是我们学习的重要目的之一。重庆一中某化学实验兴趣小组,一行四人,利用实验室老师提供的基本仪器和药品,自行购置了鸡蛋,食醋等生活用品,进行了如下探究。
I. 甲同学老家在山西,对儿时在家乡品尝到的山西老陈醋的滋味记忆犹新,跟随父母来到重庆后,总是觉得超市买到的醋不如儿时的味道,查阅相关资料后,得知以下信息:
①醋分两种,酿造醋和配制醋。正宗的老陈醋必须经长久时间酿造才得此美味,市场上多充斥着工业醋酸加水勾兑的配制醋。
②酿造醋国家标准为醋酸含量必须大于3.50 g/100mL,而配制醋国家标准仅为1.50 g~3.50g/100mL。
③在老师的帮助下,测定了超市购买的食醋中,醋酸的物质的量浓度为0.75mol/L。
(1)请帮助张同学计算从超市购买的食醋中醋酸含量为_______g/100mL,属于____________醋(填“酿造”或“配制”)。(提示:醋酸摩尔质量为60g/mol)
(2)请写出醋酸与鸡蛋壳(主要成分为CaCO3)反应的离子方程式_______________________________。
II. 下图是重庆一中化学实验室浓盐酸试剂标签上的部分内容。乙同学现用该浓盐酸配100mL1mol/L的稀盐酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:

(1)配制稀盐酸时,还缺少的仪器有?;
(2)经计算,配制100mL1mol/L的稀盐酸需要用量筒量取上述浓盐酸的体积为?mL(保留小数点后一位);
(3)对所配制的稀盐酸进行测定,发现其浓度小于1mol/L,引起误差的原因可能是?。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线