|
高考化学知识点总结《物质的量》在线测试(2019年最新版)(二)
2020-07-08 00:57:57
【 大 中 小】
|
1、选择题 NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1 L 0.2mol/LCH3COONa溶液中含有0.2NA个CH3COO―
B.标准状况下,11.2LCl2溶于水,转移的电子数为NA
C.常温常压下,23g NO2和N2O4的混合气体含有的原子数为1.5NA
D.100 mL 18.4mol/L浓硫酸与足量铜加热反应,生成SO2的分子数为0.92NA
|
参考答案:C
本题解析:A.CH3COONa是强碱弱酸盐,在溶液中CH3COO―发生水解反应变为醋酸而消耗,所以1 L 0.2mol/LCH3COONa溶液中含有CH3COO―的个数小于0.2NA个,错误;B.由于氯气溶于水,只有一部分发生反应产生盐酸和次氯酸,Cl2+H2O HCl+HClO,所以标准状况下,11.2LCl2溶于水,转移的电子数远小于0. 5NA,错误;C.常温常压下,23g NO2的物质的量是0. 5mol,含有的原子个数是1.5NA;23g N2O4的物质的量是0. 25mol,含有的原子个数是1.5NA;所以23g NO2和N2O4的混合气体含有的原子数为1.5NA,正确;D.浓硫酸能够与Cu在加热时发生反应,随着反应的进行,硫酸变稀,这时反应就不再发生所以100 mL 18.4mol/L浓硫酸与足量铜加热反应,生成SO2的分子数小于0.92NA,错误。 HCl+HClO,所以标准状况下,11.2LCl2溶于水,转移的电子数远小于0. 5NA,错误;C.常温常压下,23g NO2的物质的量是0. 5mol,含有的原子个数是1.5NA;23g N2O4的物质的量是0. 25mol,含有的原子个数是1.5NA;所以23g NO2和N2O4的混合气体含有的原子数为1.5NA,正确;D.浓硫酸能够与Cu在加热时发生反应,随着反应的进行,硫酸变稀,这时反应就不再发生所以100 mL 18.4mol/L浓硫酸与足量铜加热反应,生成SO2的分子数小于0.92NA,错误。
考点:考查阿伏加德罗常数的计算的知识。
本题难度:一般
2、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.5.6g铁粉在2.24L(标准状态)氯气中充分燃烧,失去的电子数为0.3NA
B.常温下,1 molO2和O3的混合气体中所含氧原子数为2.5NA
C.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等
D.13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
参考答案:D
本题解析:A错,铁与氯反应的方程式为:2Fe+3CL2=2FeCL3;5.6g铁粉的物质的量为0.1mol;2.24L(标准状态)氯气物质的量为0.1mol;即氯气的量不足,反应过程中失去的电子数为0.2NA;B错,由于不知道O2和O3的各自的物质的量,本题无解;C错,未指明标准状况;D正确,13.0 g锌的物质的量为0.2 mol;锌与浓硫酸反应或稀硫酸反应均为1 mol锌生成1 mol气体;
本题难度:一般
3、选择题 V mLAl2(SO4)3溶液中含有Al3+ag,取 VmL溶液稀释到4VmL,则稀释后溶液中SO42-的物质的量浓度是 VmL溶液稀释到4VmL,则稀释后溶液中SO42-的物质的量浓度是
[? ]
A. mol/L mol/L
B. mol/L mol/L
C. mol/L mol/L
D.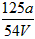 mol/L mol/L
参考答案:C
本题解析:
本题难度:简单
4、填空题 氨和联氨(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。根据题意完成下列计算:
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式为________。该氢化物受撞击则完全分解为氮气和氢气。4.30 g该氢化物受撞击后产生的气体在标准状况下的体积为________L。
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮做氧化剂,反应产物是氮气和水。由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0 kg水,则推进剂中联氨的质量________。
(3)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为6NO+ 4NH3=5N2+6H2O 6NO2+ 8NH3=7N2+12H2O。NO与NO2混合气体180 mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156 mol氮气。吸收后氨水密度为0.980 g/cm3。则①该混合气体中NO与NO2的体积比为________,②吸收后氨水的物质的量浓度________(答案保留1位小数)。
参考答案:
本题解析::(1)n(N)=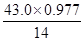 =3、n(H)= =3、n(H)= =1,因此化学式为HN3。 2HN3=H2+3N2,4.30 g HN3参加反应生成0.2 mol混合气体,标准状况下的体积为4.48 L。(2)2N2H4+N2O4=3N2+4H2O, 但当反应生成72.0 kg水时,参加反应的联氨的质量为,m(N2H4)= =1,因此化学式为HN3。 2HN3=H2+3N2,4.30 g HN3参加反应生成0.2 mol混合气体,标准状况下的体积为4.48 L。(2)2N2H4+N2O4=3N2+4H2O, 但当反应生成72.0 kg水时,参加反应的联氨的质量为,m(N2H4)= ×0.5×32 g/mol=64 000 g=64 kg。(3)设一氧化氮、二氧化氮的物质的量分别为X、Y,根据反应方程式和题干得出 ×0.5×32 g/mol=64 000 g=64 kg。(3)设一氧化氮、二氧化氮的物质的量分别为X、Y,根据反应方程式和题干得出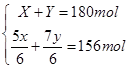 解得X=162 mol,Y=18 mol,相同条件下体积之比等于物质的量之比 解得X=162 mol,Y=18 mol,相同条件下体积之比等于物质的量之比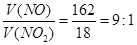 。参加反应的氨气的物质的量为 。参加反应的氨气的物质的量为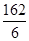 ×4+ ×4+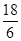 ×8=132 mol,完全反应后氨气的物质的量为 ×8=132 mol,完全反应后氨气的物质的量为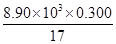 -132 mol=25 mol,完全反应后溶液的体积为 -132 mol=25 mol,完全反应后溶液的体积为
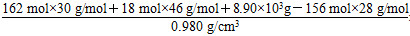 ×10-3L/cm3=10.428 L,c(NH3)=25/10.428=2.4 mol/L。 ×10-3L/cm3=10.428 L,c(NH3)=25/10.428=2.4 mol/L。
答案:(1)HN3 4.48 (2)64 kg? (3)9∶1 2.4 mol/L
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.25℃,1.01×105 Pa, 44g CO2中含有的原子数为3NA
C.1 mol Cl2与足量Fe反应,转移的电子数为3NA
D.标准状况下,11.2LH2O 含有的分子数为0.5NA
参考答案:B
本题解析:氦气是1个原子构成的,则含有NA个氦原子的氦气在标准状况下的体积约为22.4L,A不正确;B中44gCO2的物质的量是1mol,含有3mol原子,B正确;C中,转移2mol电子,不正确;D中在标准状况下,水是液态,不能适用于气体摩尔体积,D不正确,答案选B。
点评:阿伏加德罗常数是历年高考的“热点”问题,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容。要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系。
本题难度:一般
|  mol/L
mol/L  mol/L
mol/L mol/L
mol/L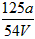 mol/L
mol/L