1、选择题 ClO2遇浓盐酸会生成Cl2?,反应方程式为2ClO2?+?8HCl?=?5Cl2?+?4H2O?,该反应中若转移电子的数目为9.632×1023,则产生的Cl2在标况下的体积为
A.11.2L
B.33.6L
C.22.4L
D.44.8L
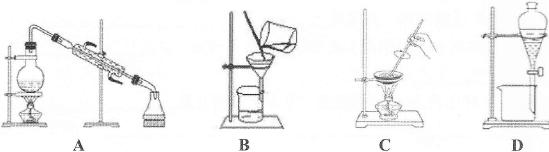
2、选择题 家里的食用玉米油不小心混入了大量的水。要将玉米油与水分离,最简便的方法是
3、选择题 高氯酸是最强的酸。60%的高氯酸溶液加热不分解,但浓度再高就不稳定,受热易分解。热浓的高氯酸遇有机物易爆炸。纯高氯酸的沸点是130℃。现在70%的商品高氯酸,为使其进一步浓缩,所采取的正确措施是
[? ]
A.加入浓H2SO4后,再小心常压蒸馏
B.加入浓H2SO4,再进行减压蒸馏
C.含仪器连接处的橡皮塞应塞紧,防止漏气
D.各仪器连接处必须用磨口玻璃装置
4、填空题 (12分)某钠盐溶液中可能含有阴离子:CO32-、SO32-、SO42-、Cl-、Br-、I-,为了鉴别这些离子,分别取少量溶液进行以下实验:
(1)加盐酸后,生成无色无味气体,该气体能使饱和石灰水变浑浊;
(2)加CCl4后,滴加少量氯水,震荡后CCl4层未变色;
(3)加BaCl2溶液后产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
(4)加稀HNO3酸化后,再加入过量AgNO3溶液,析出白色沉淀。
分析上述4个实验,写出每一步实验鉴定离子的结论与理由。
实验(1):??;
实验(2):?
?;
实验(3):??;
实验(4):??。
5、选择题 下列实验装置、试剂选用或操作正确的是( )
A.
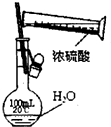
稀释浓硫酸
B.
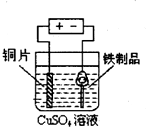
铁制品表面镀铜
C.
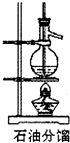
石油分馏
D.
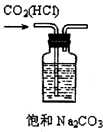
除去CO2中的HCl