1、简答题 在一定条件下,将N2和H2的混合气体100ml通入密闭容器中,达平衡时,容器内的压强比反应前减少1/5,又测得此时混合气体的平均分子量为9.试求
(1)原混合气体中N2和H2各多少毫升?
(2)H2的转化率为多少?
参考答案:(1)设原混合气体中N2的体积为x,H2的体积为y,反应中转化的N2的体积为a,则x+y=100mL ①,
N2+3H2 ?2NH3 △V
1 3 2 2
a 3a 2a
反应后气体的体积减小了2a,根据容器内的压强比反应前减少1/5,则达到平衡状态时气体的物质的量比反应前减少了15,2ax+y=15②,将①带人②解得,a=10mL,
根据三段式:N2 +3H2?2NH3
反应前:x y0
体积变化10mL30mL 20mL
平衡:x-10 y-30mL 20mL
相同条件下,气体摩尔体积相同,设为Vm,根据质量守恒定律及反应后气体的体积可得,混合气体的平均分子量为:28×xVm+2×yVmx+y-20Vm=9 ③,
由③化简有19x-7y+180=0 ④
由①④联立,解得x=20mL,y=80mL,
答:原混和气体中有N220mL,H280mL;
(2)反应消耗10mL氮气,同时消耗了30mL氢气,所以氢气的转化率为:30mL80mL×100%=37.5%,
答:H2的转化率为37.5%.
本题解析:
本题难度:一般
2、选择题 一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)  ?Y(g)+Z(s),以下能说明反应达到平衡标志的是
?Y(g)+Z(s),以下能说明反应达到平衡标志的是
A.混合气体的压强不再变化
B.X、Y、Z的物质的量之比为2:1:1
C.单位时间内生成lmolY的同时分解2mol X
D.X的分解速率与Y的消耗速率相等
参考答案:A
本题解析:在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态。平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系所以B不正确。根据方程式可知,反应前后体积是变化的,所以压强也是变化的,因此A正确。C中反应速率的方向相同,不能说明。D中反应速率的方向相反,但不满足反应速率之比是相应但化学计量数之比,不正确。答案选A。
本题难度:简单
3、选择题 取 1molA和a molB,按 A(气)+aB(气)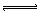 bC(气)进行反应,当A的转化率为50%时,同温同压下,测得混合气体的密
bC(气)进行反应,当A的转化率为50%时,同温同压下,测得混合气体的密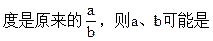
A.a=2,b=1
B.a=3,b=3
C.a=3,b=2
D.a=2,b=3
参考答案:C
本题解析:A(气) + aB(气)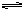 bC(气)?总
bC(气)?总
起始时物质的量(mol) ?1? a? 0? 1+a
转化的物质的量(mol) ?0.5? 0.5a? 0.5b
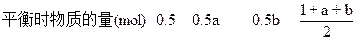

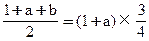
2b-a=1
讨论: 当a=1时,b=1,合理;
当a=2时,b=1.5,不合理;
当a=3时,b=2,合理;
当a>3时,选项中无。
本题难度:一般
4、选择题 在CH3COOH溶液中存在如下平衡:CH3COOH  ?H++CH3COO-,加入少量下列物质平衡不发生移动的是
?H++CH3COO-,加入少量下列物质平衡不发生移动的是
A.NaCl固体
B.CH3COONa
C.Na2CO3
D.NaOH
参考答案:A
本题解析:略
本题难度:简单
5、选择题 将5 mol O2在高温下放电,经过时间t后建立了3O2 2O3的平衡体系,已知O2的转化率为20%,下列浓度(c)变化曲线正确的是(? )
2O3的平衡体系,已知O2的转化率为20%,下列浓度(c)变化曲线正确的是(? )
参考答案:C
本题解析:由于该可逆反应是从O2开始时,故起始时O3的浓度应为0。随反应的进行,O2的浓度越来越小,其反应速率也越来越慢,而生成物中的O3的浓度越来越大。当O2的转化率达到20%时,反应达到平衡,则O2和O3的浓度不再发生变化,但平衡时,O2的浓度比O3的浓度大,故只有C图符合题意。
本题难度:简单