1、选择题 下列有关四个电化学装置的叙述正确的是
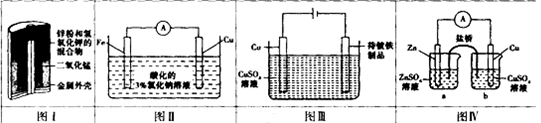
A.图I装置中MnO2作催化剂
B.图II装置工作一段时间后,滴加少量K3[Fe(CN)6]溶液,无明显现象
C.图III装置中Cu作阳极,为电解液提供Cu2+,保持溶液中Cu2+浓度恒定
D.图IV装置工作时,为平衡电荷,a烧杯中的Zn2+经盐桥移向b烧杯中
参考答案:C
本题解析:A、图I装置为碱性锌锰干电池,MnO2作正极反应物,错误;B、图II装置为原电池,铁为负极,发生氧化反应,生成亚铁离子,工作一段时间后,滴加少量K3[Fe(CN)6]溶液,变蓝色,错误;C、图III装置电镀池,Cu作阳极,为电解液提供Cu2+,保持溶液中Cu2+浓度恒定,正确;D、图IV装置为原电池,工作时,为平衡电荷,盐桥中的阳离子移向b烧杯中,错误。
本题难度:一般
2、填空题 Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是 。负极的电极反应为
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是 。欲除去Cu2+,最好选用下列试剂中的 (填代号)。
a.NaOH b.Zn c.Fe d.NH3・H2O
参考答案:(6分)(1)Zn(或锌)(1分) Zn-2e-= Zn2+(2分)
(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀(2分) b (1分)
本题解析:(1)原电池中负极失去电子,锌是活泼的金属,所以锌是负极,电极反应式是Zn-2e-= Zn2+。
(2)锌的活泼性强于铜,所以锌可以置换出铜。锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀。欲除去Cu2+,且不能再引入新的杂质,所以最好选用锌,答案选b。
考点:考查干电池的有关判断、物质的除杂
点评:该题是基础性试题的考查,试题以Zn-MnO2干电池为载体,重点考查了原电池的原理、电极反应式的书写以及物质的除杂等,有利于调动学生的学习兴趣和学习积极性,也有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确原电池的工作原理,然后灵活运用即可。
本题难度:一般
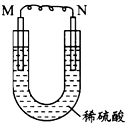
3、选择题 如图所示的装置中,M为活动性顺序位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,不正确的是
[? ]
A.N上有气体放出
B.M为负极,N为正极
C.是化学能转化为电能的装置
D.导线中有电流通过,电流方向是由M到N
参考答案:D
本题解析:
本题难度:简单
4、填空题 (8分)人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
(1)工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:

在阳极区发生的反应包括 和H ++ HCO3- ="=" H2O + CO2↑。
(2)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。
已知:25 ℃,101 KPa下:
H2(g) + 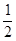 O2(g) ="==" H2O(g) Δ H1= ―242 kJ・mol-1
O2(g) ="==" H2O(g) Δ H1= ―242 kJ・mol-1
CH3OH(g) +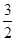 O2(g) ="==" CO2 (g) + 2 H2O(g) Δ H2= ―676 kJ・mol-1
O2(g) ="==" CO2 (g) + 2 H2O(g) Δ H2= ―676 kJ・mol-1
①写出CO2和H2生成气态甲醇等产物的热化学方程式 。
②下面表示合成甲醇的反应的能量变化示意图,其中正确的是 (填字母序号)。
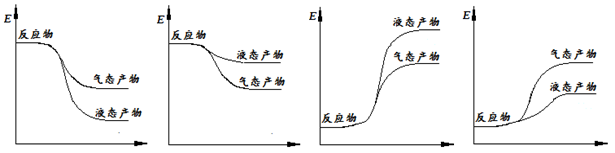
a b c d
(3)微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:

①该电池外电路电子的流动方向为 (填写“从A到B”或“从B到A”)。
②A电极附近甲醇发生的电极反应式为 。
参考答案:(1)4OH - - 4e- ="=" 2H2O + O2↑(2分)
(2)①CO2(g) + 3H2(g) ="=" CH3OH(g) + H2O(g) △H = ―50 kJ・mol-1(2分) ② a(1分)
(3) ①从A到B(1分) ②CH3OH + H2O - 6e- ="=" 6H++ CO2↑(2分)
本题解析:(1)阳极上氢氧根离子放电生成氧气和水,电极反应式为4OH--4e-
本题难度:困难
5、选择题 以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是

A.电池放电时Na+从b极区移向a极区
B.每消耗3 mol H2O2,转移的电子为3 mol
C.电极a采用MnO2,MnO2既作电极材料又有催化作用
D.该电池的负极反应为:BH4-+8OH--8e-=BO2-+6H2O