1、选择题 下列气体中选用的收集方法和干燥剂都正确的是
[? ]
A.H2----向上排空气法----碱石灰
B.O2----向下排空气法----浓硫酸
C.SO2----排水集气法----碱石灰
D.CO2----向上排空气法----浓硫酸
参考答案:D
本题解析:
本题难度:一般
2、选择题 下列气体不能用排水集气法收集的是(? )
A.NO
B.NH3
C.O2
D.CO
参考答案:B
本题解析:不能用排水法收集气体说明该气体易溶于水或能与水反应;
A,NO难溶于水且与水不反应;B氨气极易溶于水;C氧气难溶于水且与水不反应;D为CO也不水反应且难溶于水;
本题难度:简单
3、选择题 图中a、b、c表示相应仪器中加入的试剂,可用下图装置制取、净化、收集的气体是

[? ]
气体
?a
?b
c
A.
?NH3
浓氨水
生石灰
?碱石灰
B.
?CO2
盐酸
?碳酸钙
饱和NaHCO3溶液
C.
?NO
稀HNO3?
铜屑
H2O
D.
?NO2
?浓HNO3
铜屑
?NaOH溶液
参考答案:B
本题解析:
本题难度:一般
4、实验题 (14分)根据下列装置图回答问题(装置图用符号表示):
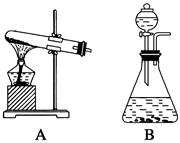
(1)双氧水(H2O2)是无色液体,可发生如下化学反应: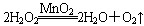 。反应中MnO2的作用是________。在实验室利用此反应制取氧气时,应选用的气体发生装置是________,简述检查本装置气密性的方法:______________________________________________。
。反应中MnO2的作用是________。在实验室利用此反应制取氧气时,应选用的气体发生装置是________,简述检查本装置气密性的方法:______________________________________________。
(2)KClO3在MnO2作催化剂时,加热也可以制得氧气。应选用的气体发生装置是________。
(3)为了验证MnO2在KClO3分解过程中起到了催化剂作用,我们要把反应后的产物分离,提取出MnO2并验证其的确是催化剂。分离出MnO2的操作有________、________、洗涤、烘干、称量。为证明MnO2是催化剂,还需要知道的一个数据是____________________。
参考答案:(1)催化剂 B 关闭分液漏斗活塞,将导气管末端插入盛水的水槽中,用手捂住锥形瓶,片刻后,导管口末端产生气泡,松开手后,末端导管上升一段水柱,则证明气密性良好 (2)A (3)溶解 过滤 加入的MnO2的质量
本题解析:本题主要考查了气体的制取原理、装置的选择、气密性的检查、物质的分离等操作。
(1)对于固液不加热的气体的制取就选用B装置,其气密性的检查见答案
(2)固固加热制取气体的发生装置为A装置。
(3)分解后试管内的物质除MnO2不溶于水外,其他的都可溶,所以可用过滤的方法分离出MnO2。
本题难度:一般
5、实验题 阿司匹林(乙酰水杨酸)是由水杨酸和乙酸酐合成的:
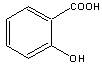 ?+ (CH3CO)2O
?+ (CH3CO)2O  ?
? ?+ CH3COOH
?+ CH3COOH
(水杨酸)? (乙酸酐)? (阿司匹林)
在生成乙酰水杨酸的同时,水杨酸分子间也能发生聚合反应,生成少量聚合物(副产物)。合成乙酰水杨酸的实验步骤如下:
①向150mL干燥锥形瓶中加入2.0g水杨酸、5mL乙酸酐(密度1.08g/ml)和5滴浓硫酸,振荡,待
其溶解后,控制温度在85~90℃条件下反应5~10min。然后冷却,即有乙酰水杨酸晶体析出。
②减压过滤,用滤液淋洗锥形瓶,直至所有晶体被收集到布氏漏斗中。抽滤时用少量冷水洗涤晶体几次,
继续抽滤,尽量将溶剂抽干。然后将粗产品转移至表面皿上,在空气中风干。
③将粗产品置于100mL烧杯中,搅拌并缓慢加入25mL饱和碳酸氢钠溶液,加完后继续搅拌2~3分钟,直到没有二氧化碳气体产生为止。过滤,用5~10mL蒸馏水洗涤沉淀,合并滤液于烧杯中,不断搅拌,慢慢加入15mL4mol/L盐酸,将烧杯置于冷水中冷却,即有晶体析出。抽滤,用冷水洗涤晶体1~2次,再抽干水分,即得产品(纯净物)1.9克。
请回答下列问题:
(1) 第①步中,要控制反应温度在85~90℃,应采用_________ 加热方法。用这种加热方法需要的玻璃仪器有?
(2) 在第②步中,用冷水洗涤晶体,其目的是?
(3) 第③步中,加入碳酸氢钠的作用是?
加入盐酸的作用是?
(4) 如何检验产品中是否混有水杨酸??
(5)试计算本次合成阿司匹林的产率为?(保留二位有效数字)
参考答案:(1)水浴,酒精灯、烧杯、温度计? (2) 洗涤晶体表面附着的杂质、减少阿司匹林因溶解而引起的损耗。(3) 使阿司匹林转化为可溶性盐,而与不溶性的物质相互分离。将阿司匹林的可溶性盐重新转化为阿司匹林。(4) 向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,产品中有水杨酸;若无紫色出现,说明产品中不含水杨酸。(5)0.80?或? 80%
本题解析:本题考查阿司匹林的合成实验。(1)水浴加热可以控制温度,需要的玻璃仪器有酒精灯、烧杯、温度计等;(2)洗涤晶体,除去表面的杂质,用冷水,目的是减小阿司匹林的溶解;(3)将阿司匹林转化为钠盐,钠盐溶于水,通过过滤而分离杂质;加入盐酸的目的是将钠盐酸化,重新转化为阿司匹林;(4)水杨酸属于酚类,通过FeCl3溶液的显色反应可以检验;(5)由2.0g水杨酸、5mL乙酸酐可以得出,乙酸酐过量,所以以水杨酸来计算,算出2.0g水杨酸能够产生阿司匹林的质量:
水杨酸~阿司匹林
138? 180
2.0? m? m=2.6g,所以阿司匹林的产率为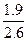 ×100%=73%。
×100%=73%。
本题难度:一般