1������� ��Al2O3��Fe2O3�Ļ�����������ʵ�飬��д������������������Ӧ�����ӷ���ʽ��
�ٽ���Ϸ�ĩ���������ܽ⣺?
������Һ���ù���Ũ��ˮ�кͣ��õ�������? ?
?
���ڳ� ���еμ�KOH��Һ����ַ�Ӧ�˳������ã�?
���еμ�KOH��Һ����ַ�Ӧ�˳������ã�?
������Һ��ͨ������CO2��?��
�ο��𰸣���? Al2O3 + 6H+��2Al3+ + 3H2O? Fe2O3 + 6H+��2Fe3+ + 3H2O
��Al3+ + 3NH3.H2O��Al(OH)3�� + 3NH4+����
Fe3+ + 3NH3��H2O��Fe(OH)3�� + 3NH4+
��Al(OH)3 + OH-��AlO2- + H2O
��AlO2- + CO2 + 2H2O��Al(OH)3 + HCO3-
�����������
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ��Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A����⻯������Һ�м���������ˮ��2I-+Br2�TI2+2Br-��
B�������������������Fe3O4+8H+�T3Fe3++4H2O
C������������ϡ���Fe2++NO3-+4H+�TFe3++NO��+2H2O
D�����Ȼ�����Һ�м����������ƣ�2?Fe3++3S2-+6H2O�T2Fe��OH��3��+3H2S��
�ο��𰸣�A����⻯������Һ�м���������ˮ���嵥�����������ӣ����ӷ���ʽΪ2I-+Br2�TI2+2Br-������A��ȷ��
B���������������������������������ӺͶ��������ӣ�Fe3O4+8H+�T2Fe3++Fe2++4H2O����B����
C������������ϡ���FeS+NO3-+4H+�TFe3++NO��+S+2H2O����C����
D�����Ȼ�����Һ�м����������Ʒ���������ԭ��Ӧ�����ӷ���ʽΪ��2Fe3++S2-=S��+2Fe2+����D����
��ѡA��
���������
�����Ѷȣ���
3��ѡ���� ���з�Ӧ�����ӷ���ʽ��д��ȷ����
[? ]
A.�Ȼ�����Һ�м��������ˮ��Al3++4NH3��H2O==?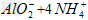 +2H2O
+2H2O
B.����ʯ��ˮ�������մ���Һ��ϣ�Ca2++OH-+HCO3-?==CaCO3��+H2O
C.̼������ڴ��CaCO3+2H+==Ca2++CO2��+H2O
D.�Ȼ�������Һ��ͨ��������2Fe2++Cl2==2Fe3++2Cl-
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ��֪��Ӧ��3NO2+H2O�T2HNO3+NO���ش��������⣺
��1���÷�Ӧ�����ӷ���ʽΪ______��
��2���������뻹ԭ����������Ϊ______�����������뻹ԭ��������ʵ���֮��Ϊ______��
��3���ڱ�״���£�3.36L?NO2��H2O��ȫ��Ӧת�Ƶĵ�����ĿΪ______��
��4���õ����ű���÷�Ӧ�е���ת�Ƶķ������Ŀ______��
��5��д��HNO3��ʯ��ˮ��Ӧ�����ӷ���ʽ______��
�ο��𰸣���1����Ӧ3NO2+H2O�T2HNO3+NO�����ӷ���ʽΪ3NO2+H2O�T2H++2NO3-+NO���ʴ�Ϊ��3NO2+H2O�T2H++2NO3-+NO��
��2����Ӧ���������е�Ԫ�ػ��ϼۼ�����Ҳ���ͣ�������������������������ԭ����3mol��NO2�У�2mol����ԭ����1mol�����������������뻹ԭ����������Ϊ1��2��
����������2NO3-����ԭ������NO���������������뻹ԭ��������ʵ���֮��Ϊ2��1���ʴ�Ϊ��1��2��2��1��
��3����Ӧ3NO2+H2O�T2HNO3+NOת�Ƶĵ���Ϊ2mol����3mol��NO2��Ӧ��ת��2mol���ӣ����ڱ�״���£�3.36L����0.15mol��?NO2��H2O��ȫ��Ӧת�Ƶĵ���Ϊ0.1mol��
��ĿΪ0.1NA���ʴ�Ϊ��0.1NA��
��4���÷�Ӧ�У�ֻ�е�ԭ�ӻ��ϼ۱仯������ת�Ƶķ������ĿΪ
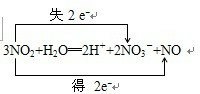
���ʴ�Ϊ��

��
��5��HNO3����ǿ�ᣩ��ʯ��ˮ����ǿ���Ӧ��������ƣ�������ˮ���Σ���ˮ�����ӷ���ʽΪH++OH-=H2O���ʴ�Ϊ��H++OH-=H2O��
���������
�����Ѷȣ�һ��
5��ѡ���� ������ʵ���Ũ�ȵ�NaHCO3��Ca(HCO3)2�Ļ����Һ�У�����һ����NaOH��Һʱ�������ܷ��������ӷ�Ӧ����ʽ��? (����)��
A��OH����HCO3��=CO32����H2O
B��Ca2����OH����HCO3��=CaCO3����H2O
C��Ca2����2OH����2HCO3��=CaCO3����2H2O��CO32��
D��Ca2����3OH����3HCO3��=CaCO3����3H2O��2CO32��
�ο��𰸣�A
�������������Һ�д���Ca2�����ʲ���������CO32������Ӧ����CaCO3������
�����Ѷȣ�һ��