1、填空题 (16分)Na、Cu、Fe、Cl、O、N是常见的6种元素。
(1)Fe位于元素周期表第_____周期第_____族;O的基态原子核外有______个未成对电子。
Cu的基态原子电子排布式为________。
(2)用“>”或“<”填空:
第一电离能
| 原子半径
| 稳定性
|
N_______O
| Cl_______Na
| NH3______H2O
|
(3)液态N2H4与液态N2O4反应生成气态水,在25℃、101kPa下,已知该反应每消耗1mol N2H4放出519.85kJ的热量,该反应的热化学反应方程式是: 。
(4)古老的但仍是最有用的制备N2H4的方法是NaClO溶液氧化过量的NH3,写出该反应的离子方程式,并标出电子转移的方向和数目 。
参考答案:(16分)
(1)四 VII (各1分) 2 (2分) 1s22s22p63s23p63d104s1或[Ar] 3d104s1(2分)
(2)> < < (各1分)
(3)N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) ?H=―1039.7kJ?mol?1 (3分)
(4)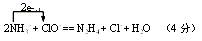
本题解析:(1)Fe元素的原子序数是26,在元素周期表中位于第四周期、第VIIA族;O原子2p分布4个电子,有2个未成对电子;CU元素的原子序数是29,基态原子电子排布式为:1s22s22p63s23p63d104s1或[Ar] 3d104s1。
(2)N原子2p轨道分布3个电子,为半充满状态,更稳定,所以第一电离能N >O;Na、Cl位于同一周期,原子序数越大,原子半径越小,则原子半径Cl<Na;O元素的非金属性大于N元素,则氢化物的稳定性NH3 < H2O。
(3)首先液态N2H4与液态N2O4反应的化学方程式,并注明状态,该反应每消耗1mol N2H4放出519.85kJ的热量,则?H=―1039.7kJ?mol?1,进而得出热化学方程式。
(4)NaClO溶液氧化过量的NH3制备N2H4,根据氧化还原反应原理和元素守恒可知同时生成Cl?和H2O,Cl元素由+1价降低为-1价,N元素由-3价升高至-2价,所以电子转移数目为2e?,可标出电子转移的方向和数目。
考点:本题考查原子结构、元素周期律与元素周期表、热化学方程式的书写、氧化还原反应原理。
本题难度:一般
2、选择题 下列有机物中,既能发生消去反应,又能发生水解反应的是
A.氯仿
B.乙醇
C.溴乙烷
D.乙酸乙酯
参考答案:C
本题解析:
本题难度:困难
3、选择题 做好环境消毒工作是预防“禽流感”的重要措施,常用的一种消毒剂是ClO2,实验室可通过以下反应制得ClO2(未配平):KClO3+H2C2O4+H2SO4
参考答案:
本题解析:
本题难度:一般
4、选择题 黑火药发生爆炸的反应中:S+2KNO3+3C==K2S+N2↑+3CO2↑被还原的元素是( )
A.只有N
B.只有S
C.只有C
D.N和S