1��ѡ���� ���и��仯������ԭ��ط�Ӧ����?��?��
A���ڿ����н���������Ѹ�������γɱ�����
B����п��Ƥ�����л���ʱ����Ȼ����ֹ��������
C�����ȵ���˿��ˮ�Ӵ��������γ�����ɫ������
D����п��ϡ���ᷴӦʱ���д������ݲ���
�ο��𰸣�B
�������������ԭ��ط�ӦҪ����ԭ��ص��γ����������Բ�ͬ�����缫���������Һ���պϵ�·����B���ϡ�Zn-Feԭ��أ�ZnΪ����������Fe��
�����Ѷȣ�һ��
2������� ����������ԭ��Ӧ��2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)��Ƶ�ԭ�������ͼ���ش��������⣺
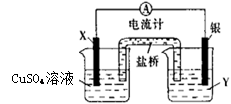
��1���缫X�IJ�����?���������ҺY��?��
��2�����缫Ϊ��ص�?����
��3����������������?�ƶ������ �����ҡ�����
��4�����·�е����Ǵ�?����缫������������ͬ���缫����?�缫��
�ο��𰸣���1��ͭ��AgNO3��Һ��2������3���ң�4��ͭ����
��������������ܷ�Ӧʽ��֪��ͼ��һ����ͭ-��ԭ��ع��죬����ͭʧ������������X�缫����Ϊ����ͭ�������ӵõ����ӱ���ԭ��������������Ӧ�������ҺΪAgNO3��Һ����������д���Cu2+ ���ɣ�����Ϊ���������Һ�����ԣ������������е������������ƶ������෴�ұߵ缫Y�д���Ag����������Ag+ �������٣���ʹ�����������������ƶ�������ͭʧȥ�ĵ��Ӵ����·ת�Ƹ����缫��
�����Ѷȣ�һ��
3��ѡ���� Ϊ̽��ԭ��ص��γ������ͷ�Ӧԭ����ijͬѧ���������ʵ�鲢��¼��������һ��Ũ�ȵ�ϡ�����в���пƬ���������������ɣ���������ϡ�����в���ͭƬ��û�п������������ɣ��۽�пƬ��ͭƬ�϶˽Ӵ�����ס��һ�����ϡ�����У�����ͭƬ�����������ɣ����������ݵ����ʱ�ʵ����п죻����пƬ��ͭƬ�м���ϵ����ƣ��ٽ�пƬ��ͭƬ����ϡ�����У����ֵ�����ָ��ƫת�����й�������ʵ����Ƽ�����ķ���������ȷ���ǣ�������
A��ʵ��١���˵��п����ϡ���ᷴӦ��ͭ����
B��ʵ���˵������ԭ��ط�Ӧʱ��ӿ컯ѧ��Ӧ����
C��ʵ���˵���ڸ�������ͭ������ϡ���ᷴӦ��������
D��ʵ���˵����ԭ�����ͭΪ������пΪ����
�ο��𰸣���пΪ���ý������������ᷢ���û���Ӧ����������
��ͭΪ�������˳�����H�Ժ�Ľ���������ϡ���ᷴӦ��
�۵�п��ͭ���Ӳ���ϡ�����У����γ�ԭ��أ�п�ϻ��ã���ԭ��صĸ������������ϲ������ģ�ͭ�ϲ����ã���ԭ��ص��������缫�������ݲ�������ԭ��ط�Ӧ��һ��Ļ�ѧ��Ӧ���ʽϴ�Ӧ��ʵ������������ͭ���ϵõ��ӱ���ԭ����������
�ܻ����Բ�ͬ��п��ͭ�Լ��������Һ�γɱպϻ�·ʱ���γ�ԭ��أ�����ѧ��ת��Ϊ���ܣ�������ָ��ƫת��
����ȷ��ֻ�Тۣ�
��ѡC��
���������
�����Ѷȣ���
4��ѡ���� ��a��b��c��d���ֽ�������a��b�õ���������������ij�������Һ�У�a�ܽ⡣��a��d�ֱ�Ͷ���Ũ�ȵ������У�d��a��Ӧ���ҡ���Cu����b������Һ������Ա仯�������Cu����c������Һ�Cu����c�ĵ����������ݴ��ж����ǵĻ����ǿ������˳����
[? ]
A.?d��a��b��c?
B.?b��a��d��c?
C.?d��b��a��c?
D.?d��c��a��b
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5��ѡ���� ����ͼʾ�ж���������������ʵ���ǣ�������
A��
���Ӻò�����Ƭ�̺���Ƭ�����һ��ͭ
B��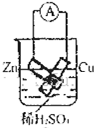
���Ӻõ��ߺ�Ƭ��Ƭ��Ӵ������������ᷢ������ƫת
C��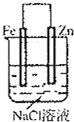
���Ӻò�����Ƭ�̺���ZnƬ������һ�η�̪��Һ����Һ��Ϊ��ɫ
D��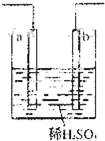
������ӦΪFe+2H+�TFe2++H2��ʱ��a��b������ͬ�ֲ��ϵĵ��
�ο��𰸣�A�����ʱ���Ʋ����������Ƽ���������������Ƭ�϶�ͭʱ��ͭ��������������������A����
B����װ���е��Ӳ��������·�����Ե�����ָ�벻ƫת����B����
C����װ���У�п�������������������缫��Ӧʽ�ֱ�Ϊ��Zn-2e-=Zn2+��O2+4e-+2H2O=4OH-���������缫������Һ��Ϊ��ɫ����C����
D����װ����ԭ��ػ���أ�ԭ���ʱ�������������������õĵ���������������ʱ�缫���Ͽ�����ͬ���Ҷ���������D��ȷ��
��ѡD��
���������
�����Ѷȣ���