1、选择题 利用如图装置,完成很多电化学实验。下列有关此装置的叙述中,正确的是(?)
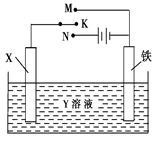
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阴离子向铁电极移动
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
参考答案:C
本题解析:A、若X为锌棒,Y为NaCl溶液,开关K置于M处,该装置为原电池,铁作正极,可减缓铁的腐蚀,这种方法称为牺牲阳极保护法,错误;B、若X为碳棒,Y为NaCl溶液,开关K置于N处,该装置为电解池,铁作阴极,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动,错误;C、若X为铜棒,Y为硫酸铜溶液,开关K置于M处,该装置为原电池,铁棒作负极,铜棒作正极,铜棒质量将增加,此时外电路中的电子向铜电极移动,正确;D、若X为铜棒,Y为硫酸铜溶液,开关K置于N处,该装置为电镀池,铁棒质量将增加,溶液中铜离子浓度不变,错误。
本题难度:一般
2、选择题 下列图示与对应的叙述不相符的是
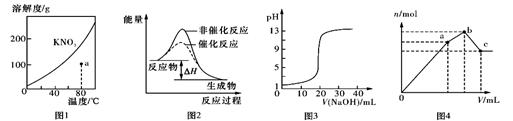
A.图1表示KNO3的溶解度曲线,a点所示的溶液是80℃时KNO3不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000mol/LNaOH滴定20.00 mL 0.1000mol/L醋酸的滴定曲线
D.图4表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,体积V与沉淀n的变化
参考答案:C
本题解析:A正确,a点位于溶解度曲线的下方,是不饱和溶液;B正确,催化剂能改变活化能,但不能改变反应热;C不正确,因为醋酸是弱酸,部分电离,存在电离平衡。所以0.1000mol/L醋酸的pH大于1,而不是等于1;应用氢氧化铝是两性氢氧化物,所以当沉淀达到最大值时,再加入氢氧化钡,沉淀会溶解,D正确,答案选C。
点评:该题容易错选D。这是由于该反应比较复杂,而选项C中的图像变化趋势又是正确的,所以错误的认为C正确,D不正确。因此把握反应的原理,既要分析曲线的变化趋势,更要注意曲线的起点和终点,只有这样才能得出正确的结论。
本题难度:一般
3、选择题 下列各组的电极材料和电解液,不能组成原电池的是( )
A.铜片、石墨棒,蔗糖溶液
B.锌片、石墨棒,硫酸铜溶液
C.锌片、铜片,稀盐酸
D.铜片、银片,硝酸银溶液
参考答案:A、蔗糖溶液不是电解质溶液,故A错误.
B、符合原电池的构成条件,故B正确.
C、符合原电池的构成条件,故C正确.
D、符合原电池的构成条件,故D正确.
故选A
本题解析:
本题难度:一般
4、选择题 下列实验操作、现象和原因解释不合理的是
选项
| 实验操作
| 实验现象
| 原因解释
|
A.
| 将一片较簿的铝片放在酒精灯火焰上灼烧
| 铝片慢慢熔化呈液滴状
| 铝表面的氧化膜致密且熔点很高,阻碍铝与氧气的接触,同时铝的熔点较低熔化了
|
B.
| 将等表面积的镁条、铝片(均除去氧化膜)分别放入装有等浓度、等体积盐酸的两支试管中
| 都产生气泡,镁条表面产生气泡更快
| 镁的金属性比铝的金属性强,镁更易失去电子,所以反应更快
|
C.
| 在打磨过的铁片上先滴一滴饱和食盐水,再滴一滴酚酞
| 液滴的外圈先出现红色
| 铁片不纯含有碳元素,铁、碳与食盐水形成原电池,溶液外圈发生吸氧腐蚀,导致c(OH-)增大,溶液呈碱性
|
D.
| 取少量淀粉加稀硫酸,加热几分钟,冷却后加入新制氢氧化铜悬浊液,加热至沸腾
| 未见砖红色沉淀生成
| 淀粉水解后没有葡萄糖生成
|
参考答案:D
本题解析:
试题分析;A、铝表面的氧化膜致密且熔点很高,阻碍铝与氧气的接触,同时铝的熔点较低熔化了,所以将一片较簿的铝片放在酒精灯火焰上灼烧铝片慢慢熔化呈液滴状,A正确;B、金属性越强越容易与酸反应反应速率越快,B正确;C、由于铁片不纯含有碳元素,铁、碳与食盐水形成原电池,溶液外圈发生吸氧腐蚀,导致c(OH-)增大,溶液呈碱性,因此在打磨过的铁片上先滴一滴饱和食盐水,再滴一滴酚酞,液滴的外圈先出现红色,C正确;D、再滴加氢氧化铜悬浊液之前首先要加入氢氧化钠中和硫酸,否则产生的葡萄糖不能用氢氧化铜悬浊液反应,D错误,答案选D。
考点:考查实验方案设计与评价
本题难度:一般
5、填空题 (5分)已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl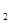 溶液、Fe
溶液、Fe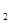 (SO
(SO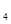 )
)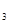 溶液、盐酸。按要求回答下列问题:若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? (填“能”或“不能”)。若能,请写出电极反应式:负极 ,正极 。若不能,请说明原因 。
溶液、盐酸。按要求回答下列问题:若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? (填“能”或“不能”)。若能,请写出电极反应式:负极 ,正极 。若不能,请说明原因 。
参考答案:
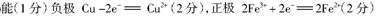
本题解析:略
本题难度:一般