1、选择题 以甲基橙为指示剂,用0.10 mol・L-1的盐酸滴定0.10 mol・L-1的氨水,
滴定过程中不可能出现的结果是(?)
A.c(NH4+)>c(Cl-),c(OH-)>c(H+)
B.c(NH4+)=c(Cl-),c(OH-)=c(H+)
C.c(Cl-)>c(NH4+),c(OH-)>c(H+)
D.c(Cl-)>c(NH4+),c(H+)>c(OH-)
参考答案:C
本题解析:解答本题时要注意两点:
(1)明确指示剂的变色范围;
(2)根据指示剂的变色范围判断滴定过程中溶液酸碱性的变化。
本题难度:一般
2、填空题 (1)由氢气和氧气反应生成1mol水蒸气放热241. 8kJ,该反应的热化学方程式为____,若1g水蒸气转化为液态水放热2.444kJ,则氢气的燃烧热为 ____ kJ/mol
(2)1.00L 1.00mol・L-1H2SO4溶液与2.00L 1.00 mol・L-1 NaOH溶液完全反应,放出114.6 kJ热量,该反应的中和热为 ____,表示其中和热的热化学方程式为___ 。
参考答案:(1)H2(g)+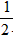 O2(g)=H2O(g) △H=-241.8kJ・mol-1 ;285. 8
O2(g)=H2O(g) △H=-241.8kJ・mol-1 ;285. 8
(2) 57. 3 kJ ・ mol-1 ;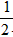 H2SO4 ( aq) + NaOH (aq) =
H2SO4 ( aq) + NaOH (aq) =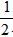 Na2SO4(aq)+H2O(l) △H = -57.3 kJ ・mol-1
Na2SO4(aq)+H2O(l) △H = -57.3 kJ ・mol-1
本题解析:
本题难度:一般
3、选择题 下列条件中可以促进水的电离的是
A.升高温度
B.加入少量固体氢氧化钾
C.加入少量固体氯化钠
D.滴加少量浓盐酸
参考答案:A
本题解析:A.升高温度,水的电离程度增大
B加入少量固体氢氧化钾,氢氧根离子浓度增大,抑制水的电离
C加入少量固体氯化钠,对水的电离无影响
D滴加少量浓盐酸,抑制水的电离。
所以促进水电离的只有A。
本题难度:一般
4、选择题 25℃时,物质的量浓度均为0.01 mol・L-1的HA和BOH溶液,pH分别为3和12,将物质的量浓度相等两溶液等体积混合后,所得溶液的pH
A.可能等于7
B.一定<7
C.一定>7
D.无法判断
参考答案:C
本题解析:物质的量浓度均为0.01 mol・L-1的HA和BOH溶液,pH分别为3和12,则HA为弱酸,BOH为强碱。等体积混合,碱过量,溶液一定呈碱性;所以正确选项为C;
本题难度:一般
5、选择题 已知某温度下,四种一元弱酸的电离平衡常数为:Ka(HCN)=6.2×10-10mol/L、Ka(HF)=6.8×10-4mol/L、Ka(CH3COOH)=1.8×10-5mol/L、Ka(HNO2)=6.4×10-6mol/L。物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是(?)
A.HCN
B.CH3COOH
C.HF
D.HNO2
参考答案:C
本题解析:电离平衡常数类似于化学平衡常熟,平衡常数越大,电离程度越大。因此根据平衡常数大小可以判断四种一元酸的相对强弱,即HF的酸性最强,所以在浓度相等的条件下,HF的酸性最强,pH最小,答案选C。
点评:对于一元弱酸,电离平衡常数越大,酸性越强,据此可以判断。
本题难度:一般