1、实验题 (8分)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是
(5)下图,是某次滴定时的滴定管中的液面,其读数为 mL
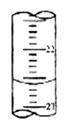
(6)根据下列数据:
滴定次数
| 待测液体积(mL)
| 标准盐酸体积(mL)
|
滴定前读数(mL)
| 滴定后读数(mL)
|
第一次
| 25.00
| 0.50
| 20.40
|
第二次
| 25.00
| 4.00
| 24.10
|
请计算待测烧碱溶液的浓度(保留四位小数) mol/L
2、选择题 关于浓度均为0.1mol?L-1的三种溶液:①CH3COOH、②NaOH、③CH3COONa溶液,下列说法不正确的是( )
A.c(CH3COO-):③>①
B.水电离出的c(OH-):②>①
C.①和②等体积混合后的溶液:c(OH-)=c(H+)+c(CH3COOH)
D.①和③等体积混合后的溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
3、选择题 常温下,某溶液中由水电离的c(H+)=1×10-13mol/L,该溶液可能是( )
①SO2水溶液,②NH4Cl溶液,③NaNO3溶液,④NaOH溶液.
A.②③
B.①④
C.③④
D.①②
4、选择题 25℃时,水的电离达到平衡:H2O 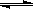 H++OH- ,下列叙述正确的是
H++OH- ,下列叙述正确的是
A. 表示的粒子不会对水的电离平衡产生影响
表示的粒子不会对水的电离平衡产生影响
B.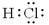 表示的物质加入水中,促进水的电离,c(H+)增大
表示的物质加入水中,促进水的电离,c(H+)增大
C.25℃时, 表示的微粒加入水中,促进水的电离,KW不变
表示的微粒加入水中,促进水的电离,KW不变
D.水的电离程度只与温度有关,温度越高,电离程度越大