1、填空题 (13分)在100℃时,将0.100 mol 的四氧化二氮气体充入 1 L 恒容真空的密闭容器中,隔一段时间对该容器内的物质浓度进行分析得到下表数据:
时间(s)
| 0
| 20
| 40
| 60
| 80
|
c(N2O4)(mol/L)
| 0.100
| c1
| 0.050
| c3
| c4
|
c(NO2)(mol/L)
| 0.000
| 0.060
| c2
| 0.120
| 0.120
|
(1)该反应的平衡常数表达式为______________________;
从表中分析:c1________c2;c3________c4(填“>”、“<”或“=”)。
(2)在下图中画出并标明此反应中c(N2O4)和c(NO2)的浓度随时间变化的曲线。
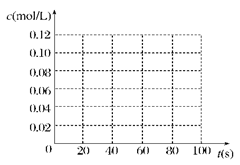
(3)在上述条件下,从反应开始直至达到化学平衡时,四氧化二氮的平均反应速率为__ mol/(L・s)。
(4)反应达到平衡后,下列条件的改变可使NO2气体的浓度增大的是
A.增大容器的容积 B.再充入一定量的N2O4
C.分离出一定量的NO2 D.再充入一定量的He
参考答案:(13分) (1)K=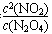 ,< , =
,< , =
(2)
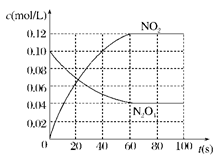
(3)0.001 (4)B
本题解析:】(1)N2O4  2NO2
2NO2
初n: 0.10 0
20s: 0.07 0.06
40s 0.05 0.10
60s: 0.04 0.12
80s: 0.04 0.12
(3)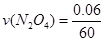 =0.001 mol/(L・s)
=0.001 mol/(L・s)
(4)增大容器的容积,各物质浓度均减少,虽然平衡略向右移,但NO2气体的浓度相对原平衡仍然是减小;而在题设条件下,恒容,分离出一定量的NO2,其浓度减少,虽然平衡略向右移,但NO2气体的浓度相对原平衡仍然是减小;再充入一定量的He,各物质浓度不变,平衡不移动;再充入一定量的N2O4,平衡正向移动,NO2气体的浓度增大,符合题意。
本题难度:一般
2、选择题 在恒容的密闭容器中,下列反应分别达到平衡后,有关说法正确的是
[? ]
A.2HI(g) H2(g)+I2(g);△H>0,若降低温度,颜色加深,压强增大
H2(g)+I2(g);△H>0,若降低温度,颜色加深,压强增大
B.2NO2(g) N2O4(g);△H<0,充入氩气,压强增大,红棕色变浅
N2O4(g);△H<0,充入氩气,压强增大,红棕色变浅
C.2SO2(g)+O2(g) 2SO3(g);△H<0,升温后,平均相对分子质量减小
2SO3(g);△H<0,升温后,平均相对分子质量减小
D.3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g);△H<0,加入铁后,Fe3O4将增加
Fe3O4(s)+4H2(g);△H<0,加入铁后,Fe3O4将增加
参考答案:C
本题解析:
本题难度:一般
3、填空题 (11分)可逆反应 ,在一定条件下达到平衡,若改 变条件,将变化情况(“增大”、“减小”、“不变”)填入空格:
,在一定条件下达到平衡,若改 变条件,将变化情况(“增大”、“减小”、“不变”)填入空格:
(1)升高温度,B转化率___________,v(正) ___________,v(逆)___________。
(2)使用催化剂,A的物质的量___________,若v(正)增大,则v(逆)____________。
(3)保持温度和压强不变加入稀有气体,则C的物质的量___________,A的转化率___________。
(4)保持温度和体积不变加入稀有气体,则A的转化率___________,v(正)_____________。
(5)若温度和体积不变,反应从正反应开始至平衡,在这个变化过程中,容器内气体的密度___________,压强___________。
参考答案:18.(1)减小;增大;增大(2)不变;减小(3)减小;减小(4)不变;不变(5)不变;减小
本题解析:(1)正反应是放热反应,所以升高温度,正逆反应速率都增大,但平衡向逆反应方向进行,B的转化率降低。(2)使用催化剂,只能加快化学反应速率,不能改变平衡,则A的物质的量不变,v(逆)减小;(3)保持温度和压强不变,加入惰性气体,则容器容积增大,所以平衡逆反应方向进行,C的物质的量和A的转化率都是减小的。(4)保持温度和体积不变,加入惰性气体,物质的浓度不变,平衡不移动,A的转化率不变,v(正)不变;(5)密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,所以容器内气体的密度不变,但压强是减小的。
考点:考查化学平衡状态及移动。
本题难度:一般
4、选择题 如图所示,反应:X(g)+3Y(g)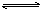 2Z(g);△H<0,在不同温度、不同压强(p1>p2)下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为
2Z(g);△H<0,在不同温度、不同压强(p1>p2)下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为
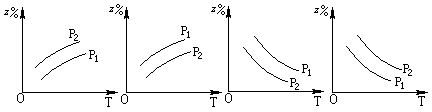
A.?B.? C.? D.
参考答案:C
本题解析:根据反应可知,该反应为放热反应,且反应物计量数之和大于生成物计量数。增大压强,Z百分含量应增大,升高温度Z百分含量降低。选项中C图像符合,故选择C选项。
本题难度:一般
5、填空题 (12分)汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g) + O2(g)  2NO(g) △H > 0已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
2NO(g) △H > 0已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5 mol,则N2的反应速率 。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志 。
A.消耗1molN2同时生成1molO2
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.2V(N2)正=V(NO)逆