1、填空题 在一定条件下,xA+yB?zC,达到平衡,试填写下列空白:
(1)若A、B、C都是气体,减压后向逆反应方向移动,则x、y、x之间的关系是______.
(2)已知C是气体,且x+y=z,加压时平衡如果发生移动,则平衡必向______方向移动.
(3)若B、C是气体,其他条件不变时增加A的用量,平衡不移动,则A的状态为______.
(4)加热后C的百分含量减少,则正反应是______反应(选填“吸热”、“放热”)
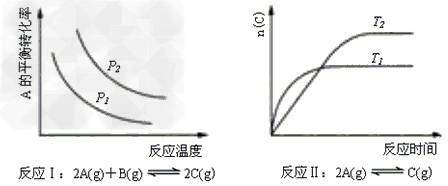
2、选择题 某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P 表示压强,T 表示温度,n 表示物质的量):根据以上规律判断,上列结论正确的是
[? ? ]
A.反应Ⅰ:△H>0,P2>P1?
B.反应Ⅱ:△H>0,T1>T2
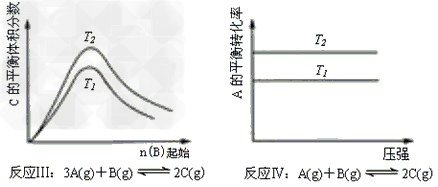
C.反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1?
D.反应Ⅳ:△H<0,T2>T1
3、填空题 (14分)已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃
| 700
| 800
| 830
| 1000
| 1200
|
平衡常数
| 1.7
| 1.1
| 1.0
| 0.6
| 0.4
|
请回答下列问题:
(1)该反应平衡常数表达式为K=______ ;ΔH___0(选填“>”、“<”或“=”)。
(2)830 ℃时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,若测得反应初始至6 S内A的平均反应速率v(A)=0.003 mol ・ L-1・ S-1,则6 S时c(A)=______ mol・L-1;C的物质的量为______ mol 。
(3)在与(2)相同的温度、容器及A、B配比下反应经一段时间后达到平衡,此时A的转化率为______;如果这时向该密闭容器中再充入1 mol氩气,则平衡时A的转化率______ (选填“增大”、“减小”、“不变”)。
(4)判断该反应是否达到平衡的依据为______(填正确选项的字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(5)1200 ℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为______ 。
A(g)+B(g)的平衡常数的值为______ 。
4、填空题 氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化。
(1)对反应2NO2(g) N2O4(g)? △H=-57.2kJ・mol-1
N2O4(g)? △H=-57.2kJ・mol-1
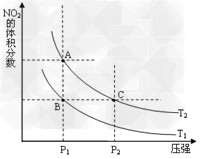
①在温度为T1、?T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1_____T2 (填“大于”、“小于”或“等于”);
②A、C两点气体的平均相对分子质量:A_____C(填“大于”、“小”或“等于”)
(2)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据
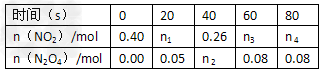
①在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为_____________。
②该条件下平衡常数K的值为______________。?
③若其他条件不变,下列既能加快正反应速率又能提高NO2转化率的措施是_______
A.抽出N2O4?B.降低温度?C.加压?D.加入催化剂?
④若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始的物质的量是________。
⑤若其它条件不变,只将容器改为带活塞的恒压容器,则平衡时N2O4的量_______0.08mol。(填“大于”、“小于”或“等于”)
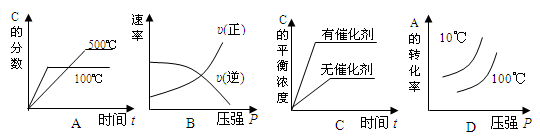
5、选择题 对于可逆反应: 2A(g)+B(g)  2C(g) △H<0,下列各图中正确的是
2C(g) △H<0,下列各图中正确的是