1、选择题 在2A+B 3C+4D反应中,表示该反应速率最快的是?
3C+4D反应中,表示该反应速率最快的是?
[? ]
A.v(A)=?0.5?mol/(L・s)?
B.v(B)=?0.3?mol/(L・s)
C.v(C)=?0.8?mol/(L・s)?
D.v(D)=?1?mol/(L・s)
参考答案:B
本题解析:
本题难度:简单
2、选择题 下列说法正确的是(?)
A.化学反应中化学能只可以转化为热能
B.可逆反应达到平衡后,正、逆反应速率均为0
C.N?2和H2反应达到平衡后,无N?2或H2剩余
D.化学反应中一定有化学键的断裂和形成
参考答案:D
本题解析:在化学变化中好想你也可以转化为其它形式的能,例如光能,A错误。可逆反应达到平衡后,正、逆反应速率相等,但不为0,B错误。可逆反应的转化率不可能是100%的,因此平衡后,一定有氮气和氢气。选项D属于化学变化的本质,正确,答案D。
本题难度:一般
3、选择题 一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g) C(g)+D(g)已达平衡状态的是
C(g)+D(g)已达平衡状态的是
A.混合气体的压强不随时间变化而变化B.气体总物质的量不随时间变化而变化
C. 2 v (B)正=v (D)逆?D.单位时间内消耗n mol C,同时消耗2nmol B
参考答案:D
本题解析:该反应前后气体的物质的量是不变的,因此在反应过程中压强始终是不变的,A、B均不能说明。在选项C中虽然反应方向是相反的,但速率之比不满足相应的化学计量数之比,也不能说明。在D中反应方向是相反,且满足速率之比是相应的化学计量数之比,故可以说明反应已达到平衡状态。答案D。
本题难度:一般
4、填空题 将1 mol I2(g) 和2 mol H2置于2L密闭容器中,在一定温度下发生反应:
I2(g) + H2(g)  ?2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示
?2HI(g);△H<0,并达平衡。HI的体积分数w(HI)随时间变化如图曲线(Ⅱ)所示
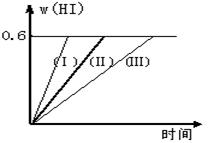
(1)达平衡时,I2(g)的物质的量浓度为?写出该反应的平衡常数表达式? _____________________________________。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ) 所示,在乙条件下w(HI)的变化如曲线(Ⅲ) 所示。则甲条件可能是?,则乙条件可能是??。
(填入下列条件的序号)
①恒容条件下,升高温度;? ②恒容条件下,降低温度;③恒温条件下,缩小反应容器体积;? ④恒温条件下,扩大反应容器体积;? ⑤恒温恒容条件下,加入适当催化剂。
参考答案:(1) 0.05mol/L;K=[HI]2/[H2][I2]?(2) 3、5;4
本题解析:(1)由于该反应前后气体体积不变,所以根据图像可知,平衡时HI的物质的量是3mol×0.6=1.8mol,则消耗单质碘的物质的量是0.9mol,所以平衡时I2(g)的物质的量浓度为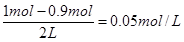 ;化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此根据反应的化学方程式可知,该反应的平衡常数K=[HI]2/[H2][I2]。
;化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此根据反应的化学方程式可知,该反应的平衡常数K=[HI]2/[H2][I2]。
(2)曲线(Ⅰ)和曲线(Ⅱ)相比,HI的含量不变,即平衡状态不变,但到达平衡的时间减少。这说明反应速率加快,所以改变的条件应该是恒温条件下,缩小反应容器体积或恒温恒容条件下,加入适当催化剂,答案选③⑤;曲线(Ⅲ) 和曲线(Ⅱ)相比,HI的含量不变,即平衡状态不变,但到达平衡的时间增加。这说明反应速率降低,所以改变的条件应该是恒温条件下,扩大反应容器体积,答案选④。
点评:本题是高考中的常见题型,属于中等难度的试题,试题基础性强,难易适中。本题主要是检验学生对基础知识的理解掌握程度,以及图像识别、分析、归纳问题的能力,本题学生不难得分。
本题难度:困难
5、选择题 在一定条件下,测得2CO2 2CO+O2(反应从CO2开始)平衡体系的平均相对分子质量为M,在此条件下,CO2的分解率为?(?)
2CO+O2(反应从CO2开始)平衡体系的平均相对分子质量为M,在此条件下,CO2的分解率为?(?)
A.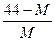 ? B.
? B.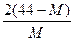 ? c.
? c.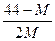 ? D.
? D.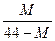
参考答案:B
本题解析:略
本题难度:简单