1、简答题 下表为长式周期表的一部分,其中的编号代表对应的元素.

试填空.
(1)写出上表中元素⑨原子的外围电子排布式______.
(2)元素③与⑧形成的化合物中元素③的杂化方式为:______杂化,其形成的化合物的晶体类型是:______.
(3)元素④、⑤的第一电离能大小顺序是:______>______(用元素符号表示);元素④与元素①形成的X分子的空间构型为:______.请写出与N3-互为等电子体的分子、离子的化学式______,______(各写一种).
(4)在测定①与⑥形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:______.
(5)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质,写出元素②的氢氧化物与NaOH溶液反应后盐的化学式______.
(6)元素⑩在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为______.

2、填空题 原子序数依次递增的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期。已知X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼铁;Z与X同主族,其单质在同周期元素形成的单质中熔点最高;W原子M能层为全充满状态,且核外的未成对电子只有一个。回答下列问题:
(1)X能形成多种常见单质,其熔点最低的单质为___晶体;在熔点最高的两种单质中,X的杂化方式分别为 ____、____。
(2)X、Y分别与氢元素形成的化学键的极性大小为X-H____Y-H,键能大小为X-H____Y-H(填“<”、 “>”或“=”)。
(3)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有 I3、I4、I5…,推测Z元素的电离能突增应出现在第___电离能。
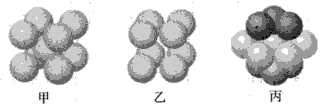
(4)W原子的电子排布式为___;W基态原子有___种不同形状的原子轨道;W晶体的配位数为____;下图___表示的是W晶体中原子的堆积方式(填“甲”、“乙”或“丙”)。
(5)向W的硫酸盐溶液中逐滴滴加氨水至过量,最终形成的化合物中含___键(填化学键 类型)。
3、选择题 下列叙述中,正确的是( )
A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子
B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子
C.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高
D.如果某一基态3p能级上仅有2个电子,它们自旋方向必然相反
4、选择题 下列各分子中,所有原子都满足最外层为8电子结构的是( )
A.H2O
B.BF3
C.CCl4
D.HCl
5、填空题 目前科学家们正在研究开发新型制冷剂,如“磁制冷剂”。已知磁制冷剂的原子中常具有较多的未成对电子,在磁场作用下,电子自旋方向从一致到不一致就会从环境吸热而制冷。美、中等国家已开始这方面的研究,并于2002年制成第一台磁冰箱。研究者最先采用的磁制冷剂是稀土金属钆(64Gd),我国有丰富的储藏。已知54号元素是Xe。请你帮助分析为什么电子自旋方向发生变化能制冷,写出稀土金属钆的核外电子排布式和轨道表达式,并确定未成对电子数。
__________________________________________