1、填空题 超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO2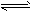 CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表
CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表
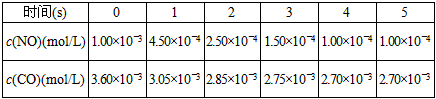
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H___________0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=______________。
(3)在该温度下,反应的平衡常数K=________________。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________________。
A.选用更有效的催化剂 B.升高反应体系的温度 C.降低反应体系的温度 D.缩小容器的体积
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。

|
(5)请在上表空格中填入剩余的实验条件数据。
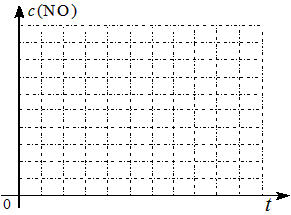
(6)请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号。
2、简答题 某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.
(1)该反应的离子方程式为(提示:H2C2O4的一级电离常数为5.4×10-2)______.
(2)实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol?L-1、0.001mol?L-1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1mol?L-1)的用量均为2mL.如果要探究反应物浓度、温度、催化剂对反应速率的影响,通过变换这些实验条件,至少需要完成______个实验进行对比即可得出结论.
(3)在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
KMnO4酸性溶液
的浓度/mol?L-1 | 溶液褪色所需时间?t/min
第1次
第2次
第3次
0.01
14
13
11
0.001
6
7
7
|
①计算用0.001mol?L-1?KMnO4酸性溶液进行实验时KMnO4的平均反应速率(忽略混合前后溶液的体积变化,写出计算过程).
②若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?______.若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案:______.
3、选择题 下图是可逆反应A+2B  ?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断

A.正反应是吸热反应
B.若A、B是气体,则D是液体或固体
C.D可能是气体.
D.A、B、C、D均为气体
4、选择题 某温度下,将2 mol A和1 mol B放入一密闭容器中,发生反应:A(g)+B(g) 2C(s)+2D(g),5 min后反应达到平衡,测得生成C为0.8 mol,下列相关表述正确的是
2C(s)+2D(g),5 min后反应达到平衡,测得生成C为0.8 mol,下列相关表述正确的是
A.该反应的化学平衡常数表达式是K=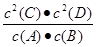
B.若向平衡体系中加入少量生成物C,则正、逆反应速率均增大
C.增大该体系的压强,A的转化率增大
D.该条件下B的平衡转化率是40%