1、实验题 (10分)有一份铵盐混合物,取其质量为10.00g时,含有xmol的(NH4)2SO4和ymol的NH4HSO4 。以下实验取用不同质量的铵盐混合物均加入同浓度的50.00mL的NaOH溶液, 加热充分反应,将产生的气体A经干燥之后用浓硫酸吸收。
。以下实验取用不同质量的铵盐混合物均加入同浓度的50.00mL的NaOH溶液, 加热充分反应,将产生的气体A经干燥之后用浓硫酸吸收。
测定结果如下;
铵盐混合物质量为10.00g和20.00g时,浓硫酸增加的质量相同;
铵盐混合物质量为30.00g时,浓硫酸增加的质量为0.68g;
铵盐混合物质量为40.00g时,浓硫酸的质量不变。
(1)A气体的化学式为______________
(2)10.00g铵盐混合物中含有NH4+的物质的量为_____mol(用含x,y的关系式表示),10.00g铵盐混合物溶于水后可电离出H+的物质的量为___mol(用含x,y的关系式表示)。
(3)在含有2 mol NH4+与1 mol H+的溶液中加入2 molOH―,加热充分反应,可产生气体A__________ mol
(4)计算:50.00mL的NaOH溶液的浓度为__________mol/L,该铵盐中氮元素的质量分数是?%;(计算结果均保留两位小数)
参考答案:(10分)(1)NH3(2分)
(2)2x+y;y(2分)
(3)1(2分)
(4)4.64mol/L,;14.56%(4分)
(参考解法,解题过程不计入评卷总分, 设氢氧化钠的物质的量浓度为Cmol/L,
设氢氧化钠的物质的量浓度为Cmol/L, 设10克中有Xmol的 (NH4)2SO4和ymol的NH4HSO4则
设10克中有Xmol的 (NH4)2SO4和ymol的NH4HSO4则 132X + 115y=10.(1)
132X + 115y=10.(1)
 10g时说明铵盐不足,?
10g时说明铵盐不足,? 20g时铵盐已经过量,
20g时铵盐已经过量,  ?n(NH3)="2X" + y=50C×10―3―2y.(2)
?n(NH3)="2X" + y=50C×10―3―2y.(2)
 30g时铵盐过量,
30g时铵盐过量,  ?
? ?50C×10―3―3y=0.68/17.(3)
?50C×10―3―3y=0.68/17.(3)
 联立(1) (2) (3)解得
联立(1) (2) (3)解得 ? X=0.02mol? y=0.064mol? C=4.64mol/L
? X=0.02mol? y=0.064mol? C=4.64mol/L
 氮的质量分数="(0.04+0.064)" ×14/10×100%=14.56% )
氮的质量分数="(0.04+0.064)" ×14/10×100%=14.56% )
本题解析:(1)每次所用氢氧化钠的量相同,根据10克铵盐混合物中含有xmol的(NH4)2SO4和ymol的NH4HSO4。则有20克铵盐混合物中含有2xmol的(NH4)2SO4和2ymol的NH4HSO4。这里消耗氢氧根离子有氢离子和铵离子,而且是中和反应在前,反应的离子方程式为:H++OH- =H2O,NH4++OH- NH3↑+H2O,产生的气体A为氨气,化学式为NH3。
NH3↑+H2O,产生的气体A为氨气,化学式为NH3。
根据10克混合物和20克混合物得到等量的氨气,说明在和10克混合物反应时,氢氧化钠过量,和20克反应时氢氧化钠不足。40克时说明只发生了氢氧根和氢离子的反应。xmol的(NH4)2SO4和ymol的NH4HSO4,生成氨气2x+y,消耗氢氧化钠2x+2y,2xmol的(NH4)2SO4和2ymol的NH4HSO4,生成氨气2x+y,消耗氢氧化钠2y+2x+y。
(2)混合物质量是30克时,含有3xmol的(NH4)2SO4和3ymol的NH4HSO4.根据20克时氢氧化钠不足,说明氢氧化钠的物质的量为3y+2x,减去氢离子消耗的氢氧化钠就是产生的氨气的量,即:3y+2x-3y="0.68/17" 摩尔, x="0.02mol," 在根据 132x+115y=10克,解y=0.064摩尔。所以10.00克铵盐混合物中含有NH4+的物质的量:0.02*2+0.064="0.104mol" .10.00克铵盐混合物溶于水后可电离出H+的物质的量0.064mol。
(3)在含有2 mol? NH4+与1 mol H+的溶液中加入2 mol OH-,加热充分反应,氢氧根先中和1摩尔氢离子,剩余的1摩尔氢氧根离子和1摩尔的铵离子反应得到氨气1摩尔。
(4)NaOH溶液的浓度为(3y+2x)/0.05? =(3*0.064+2*0.02)/0.05=4.64摩尔/升。
该铵盐中氮元素的质量分数= (0.064+2×0.02)×14/10.00=14.56%。
点评:本题考查的是化学计算,考查学生的问题分析能力以及计算能力,本题涉及的内容为氨及铵盐之间的反应。化学计算需注重解题技巧。
本题难度:一般
2、选择题 下列在限定条件溶液中的各组离子,能够大量共存的是
A.pH=3的溶液:Na+、Cl-、Fe2+、ClO-
B.与Al能产生氢气的溶液:K+、SO42-、CO32-、NH4+
C.使酚酞试液变红的溶液: Na+、Cl-、SO42-、Al3+
D.水电离的H+浓度为1×10-12 mol・L-1的溶液:K+、Ba2+、Cl-、Br-
参考答案:D
本题解析:A 错误,pH=3是酸性环境,Fe2+、ClO-不能大量共存
B 错误,与Al能产生氢气的溶液可能显酸性或碱性,在酸性环境下,CO32-不能共存,在碱性环境下,NH4+不能共存
C 错误,使酚酞试液变红的溶液显碱性,Al3+不能大量共存
D 正确,在酸性、碱性中都能大量共存
本题难度:简单
3、选择题 常温下,下列各组离子在有一定关限定条件下的溶液中一定能大量共存的是
A.由水电离产生的c(H+)=10-12 mol・L一1的溶液中:K+、Na+、Fe2+、NO3-
B.常温下,pH=7的溶液中: Al3+、Cl-、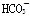 、SO42-
、SO42-
C.常温下,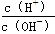 =1×10-12的溶液:K+、Cu2+、S2-、Cl-
=1×10-12的溶液:K+、Cu2+、S2-、Cl-
D.pH=13的溶液中:K+、Ba2+ 、Cl-、OH-