|
�߿���ѧ֪ʶ����ɡ����ӹ��桷���⼼�ɣ�2019�����°棩(��)
2020-07-08 01:50:01
�� �� �� ��
|
1��ѡ���� ����ʱ�����и���������ָ����Һ�п��Դ���������ǣ�������
A����ˮ�������c��H+��=10-12mol/L����Һ�У�Na+��Ba2+��HCO ��C1-
B����ɫ����Һ�У�K+��Cu2+��SO��Na+
C�����д���AlO2-����Һ�У�Na+��OH-��Cl-��CO
D����ʹpH��ֽ�Ժ�ɫ����Һ�У�Na+��ClO-��Fe2+��SO
�ο��𰸣�A����ˮ�������c��H+��=10-12mol/L����Һ��Ϊ������Һ��HCO3-�������ᷴӦ������Ӧ����һ�����ܹ��棬��A����
B��Cu2+Ϊ��ɫ������ɫ��Һ��������B����
C�����д���AlO2-����Һ���Լ��ԣ���������֮�䲻��Ӧ���ܹ��棬��C��ȷ��
D����ʹpH��ֽ�Ժ�ɫ����Һ�������ԣ�Fe2+��ClO-��H+����֮�䷢��������ԭ��Ӧ�����ܹ��棬��D����
��ѡC��
���������
�����Ѷȣ�һ��
2������� ij��ɫ����Һ�п��ܴ�������Ag����Mg2����Cu2����Fe3����Na���еļ��֣�����д���пհף�
(1)�����κ�ʵ��Ϳ��Կ϶�ԭ��Һ�в����ڵ������� ��
(2)ȡ����ԭ��Һ���������ϡ���ᣬ�а�ɫ�������ɣ��ټ��������ϡ���ᣬ��������ʧ��˵��ԭ��Һ�п϶����ڵ������� ���йص����ӷ���ʽΪ ��
(3)ȡ(2)�е���Һ�����������ϡ��ˮ(NH3��H2O)�����ְ�ɫ������˵��ԭ��Һ�п϶��� ���йص����ӷ���ʽΪ ��
(4)ԭ��Һ���ܴ������ڵ������������е� ��
A��Cl��
B��NO3��
C��CO32��
D��OH��
|
�ο��𰸣�(1)Cu2����Fe3����(2)Ag����Ag����Cl��=AgCl��
(3)Mg2����Mg2����2NH3��H2O=Mg(OH)2����2NH4����(4)B
���������(1)��ɫ����Һ�в����ܺ���Cu2����Fe3������ɫ���ӡ�(2)��ϡ�����в�����ϡ����İ�ɫ�������ɣ���϶�����Ag�������ӷ���ʽΪAg����Cl��=AgCl����(3)��ϡ��ˮ�а�ɫ�������֣��϶�����Mg2����(4)ԭ��Һ�����ں���Ag�����������в����ܺ���Cl����CO32����OH�������ܺ�NO3����
�����Ѷȣ�һ��
3��ѡ���� �ڼס������ձ���Һ�У����д�����Cu2+��Na+��H+��SO42-��CO32-��OH-��6�����ӡ���֪���ձ�����Һ����ɫ�������ձ�����Һ�д������ڵ�������
[? ]
A��Cu2+��H+��SO42-
B��Na+��OH-��CO32-
C��CO32-��OH-��SO42-
D��Na+��H+��SO42-
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4������� ���û�ѧԭ�����ԶԹ����ŷŵķ�ˮ�������Ƚ�����Ч��������������ij�������Ƹ﹤ҵ������Cr(III)�Ĵ����������£�
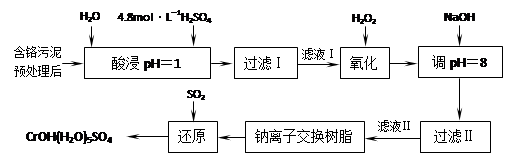
���������ȡҺ�еĽ���������Ҫ��Cr3+�������Fe3+��Al3+��Ca2+��Mg2+��
��1��ʵ������18.4 mol��L�D1��Ũ��������250 mL 4.8 mol��L�D1��������Һ�����õIJ����������ձ����������ͽ�ͷ�ι��⣬����???��
��2�����ʱ��Ϊ����߽�ȡ�ʿɲ�ȡ�Ĵ�ʩ��???��
???��(д��������ʩ)
��3��H2O2�������ǽ���Һ���е�Cr3+ת��ΪCr2O72�D��д���˷�Ӧ�����ӷ���ʽ��
???��?
��4�������£�����������������������ʽ����ʱ��Һ��pH���£�
������
| Fe3+
| Mg2+
| Al3+
| Cr3+
| ��ʼ����ʱ��pH
| 2.7
| ����
| ����
| ����
| ������ȫʱ��pH
| 3.7
| 11.1
| 8
| 9����9�ܽ⣩
|
?
����NaOH��Һʹ��Һ�ʼ��ԣ�Cr2O72�Dת��ΪCrO42�D����Һ������������Ҫ��?������Һ��pH���ܳ���8����������?��
��5�������ӽ�����֬�ķ�Ӧԭ��Ϊ��Mn+��nNaR��MRn��nNa+�����������ӽ�����֬��ȥ��Һ���еĽ�����������???��
��6��д��������������SO2���л�ԭ�Ļ�ѧ����ʽ?��
�ο��𰸣���1��250mL����ƿ��1�֣�����Ͳ��1�֣�
��2�����߷�Ӧ�¶ȡ������������ı�������ӿ�����ٶȵȣ�3���д�2�㼴��2�֣�
��3��2Cr3+ + 3H2O2 + H2O ��? Cr2O72��+ 8H+��2�֣�
��4��Na+��Mg2+��Ca2+��2�֣�
pH����8��ʹ����Al(OH)3�ܽ�����AlO2��������Ӱ��Cr(III)�����������ã�2�֣�
��5��Ca2+��Mg2+��2�֣�
��6��3SO2 + 2Na2CrO4 + 12H2O �� 2CrOH(H2O)5SO4��+ Na2SO4 + 2NaOH ��2�֣�
��3SO2 + 2CrO42�� + 12H2O �� 2CrOH(H2O)5SO4��+ SO42�� + 2OH����
�����������1���������ʵ���Ũ�ȵ����ơ�����������������֪����ȱ��250ml����ƿ����Ͳ��
��2��������������Է�Ӧ���ʵ�Ӱ�졣�ɴ��¶ȣ�Ũ�ȺͽӴ�����ȽǶȽ��п��ǡ�
��3������������ԭ��Ӧ����ʽ����ƽ�����ݵ�ʧ�����غ������ƽ��
��4�����ݳ���ʱ��pHֵ�����жϣ���pH��8ʱ����Һ�е�Fe3+��Al3+�Ѿ�����������������γ���������Һ�е���������Ҫ����Na+��Mg2+��Ca2+����ΪpH̫�ߣ����ܽ���������������Ӱ�������ʵ��ķ�����ᴿ��
��5�����������ӽ�����֬�ķ�Ӧԭ����֪����Һ�е�Ca2+��Mg2+������������ȥ��
��6���������ʷ�Ӧǰ��ı仯��֪����������������ԭ��Һ�е�CrO42�D���仹ԭ������CrOH(H2O)5SO4��Ȼ����ݵ�ʧ�����غ���ƽ���ɡ�
�����Ѷȣ�һ��
5��ѡ���� �ס�������Һ�У��ֱ��д�����Cu2����K����H����Cl����CO32����OH��6�������е�3�֣���֪����Һ����ɫ��������Һ�д������ڵ�������(����)
A��K����OH����CO32��
B��Cu2����H����Cl��
C��K����H����Cl��
D��CO32����OH����Cl��
�ο��𰸣�A
����������ɼ���Һ����ɫ��˵������Cu2����OH����CO32���ز������ڼ���Һ�У�������������Һ�У�H����OH�����ܴ������棬��H���ش����ڼ���Һ�У�������Һ�ĵ����ԣ�����Һ�бغ���һ�������ӣ�ֻ��ΪK����������Һ�д������ڵ�����ΪK����OH����CO32��
�����Ѷȣ�һ��
|