1、选择题 在1L0.3mol・L-1的NaOH溶液中,通入标准状况下的4.48LCO2,完全反应后,下列关系式正确的是
[? ]
A.C(Na+)>C(OH-)>C(CO32-)>C(H+)>C(OH-)
B.C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+)
C.C(Na+)>C(CO32-)>C(HCO3-)>C(OH-)>C(H+)
D.C(Na+)+C(H+)=C(OH-)+C(HCO3-)+2C(CO32-)
参考答案:BD
本题解析:
本题难度:一般
2、选择题 常温下,将aL0.1 mol/L的NaOH溶液与 b L0.l mol/L的CH3COOH溶液混合,下列有关混合溶液的说法不正确的是
[? ]
A.a<b时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.a>b时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.a=b时,c(CH3COOH)+c(H+)=c(OH-)
D.无论a、b有何关系,均有c(H+)+c(Na+)= c(CH3COO-)+c(OH-)
参考答案:B
本题解析:
本题难度:一般
3、简答题 化学兴趣小组的同学将Na2SO3在隔绝空气并经600℃以上的强热至恒重,然后对加热后固体进行元素定性定量分析,确定固体组成与Na2SO3无异;但把加热后固体溶于水,得到的溶液pH值比Na2SO3溶液的pH高.
(1)Na2SO3溶液呈______性(填“酸”或“碱”),其原理是(以相关的离子方程式表示)______.
(2)强热后的物质是什么呢?同学作如下探究
①分析猜想:Na2SO3在强热下发生了分解反应(自身氧化还原反应)
②该残留物可能的存在物质:
假设1:______;
假设2:______.
③设计实验方案证明你的假设,请按下表格式完成相关内容.(限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、试管夹;6mol?L-1?HCl、0.1mol?L-1BaCl2、0.1mol?L-1KCl、蒸馏水)
| 实验步骤 | 预期现象和结论
步骤1:取少量固体分别于试管中,加入一定量的蒸馏水溶解
固体全部溶解
步骤2:
步骤3
参考答案:(1)Na2SO3为强碱弱酸盐,SO32-水解呈碱性,水解的离子方程式为SO32-+H2O?

?HSO3-+OH-,
故答案为:碱;SO32-+H2O?

?HSO3-+OH-;
(2)②Na2SO3在强热下发生了自身氧化还原反应,化合价升高可生成Na2SO4,说明化合价降低生成可能生成S或Na2S,产物全部溶于水,得到的溶液pH值比Na2SO3溶液的pH高,
说明生成Na2S,
则有两种可能:如全部发生分解反应,则生成Na2S?和Na2SO4;如部分发生分解反应,则有Na2S、Na2SO3?和Na2SO4存在,
故答案为:Na2S?和Na2SO4;Na2S、Na2SO3?和Na2SO4;
③如固体中含有Na2S和Na2SO3,在酸性条件下发生:SO32-+2S2-+6H+=3S↓+3H2O,则溶液变浑浊,如仅有特殊气味的气体放出,说明固体中含有Na2S,发生:S2-+2H+=H2S↑;
然后取反应后的澄清溶液滴加0.1?mol?L-1BaCl2溶液,若有白色沉淀生成,则说明固体中含有Na2SO4.否则假设1成立,
故答案为:
实验步骤预期现象和结论步骤2:往试管中,加入足量6?mol?L-1?HCl若溶液变浑浊,则说明固体中含有Na2S和Na2SO3;若溶液没有变浑浊,而仅有特殊气味的气体放出,说明固体中
含有Na2S步骤3:取步骤2中的澄清液于试管,然后往试管中加入少量0.1?mol?L-1BaCl2若有白色沉淀生成,则说明固体中含有Na2SO4.结合步骤2,若溶液没有变浑浊,只有气体放出,则假设1成立;若溶液变浑浊,则假设2成立.
本题解析:
本题难度:一般
4、填空题 北京奥运会"祥云火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。已知:
C3H8(g)==CH4(g)+HC≡CH(g)+H2(g) △H1=156.6kJ/mol
CH3CH=CH2(g)==CH4(g)+HC≡CH(g)?△H2=32.4kJ/mol?
则相同条件下,反应C3H8(g)==CH3CH=CH2(g)+H2(g)的△H=__________kJ/mol?
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷.电解质是熔融碳酸盐。电池反应方程式为___________________;放电时,CO32-移向电池的__________(填“正”,或“负”)极。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2,溶于水达到平衡时,溶液的pH=5.6,c(H2CO3)=l.5×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3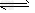 HCO3-+H+的平衡常数K1=?_______。(已知:10-5.60=2.5×10-6) HCO3-+H+的平衡常数K1=?_______。(已知:10-5.60=2.5×10-6)
(4)常温下,0.1mol/LNaHCO3溶液的pH大于8,则溶液中c(H2CO3)?______c(CO32-)(填“>”、“=”或“<”),原因是______________(用离子方程式和必要的文字说明)。
参考答案:(1)124.2
(2)C3H8+5O2=3CO2+4H2O;负
(3)4.2×10-7mol/L
(4)>;HCO3-+H2O CO32-+H3O+(或HCO3- CO32-+H3O+(或HCO3- CO32-+H+),HCO3-+H2O CO32-+H+),HCO3-+H2O H2CO3+OH-,HCO3-的水解程度大于电离程度 H2CO3+OH-,HCO3-的水解程度大于电离程度
本题解析:
本题难度:一般
5、选择题 100mL?0.1mol/L的盐酸与50mL?0.2mol/L的氨水混合,充分反应后,所得溶液中各种离子浓度关系正确的是( )
A.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.c(Cl-)=c(NH4+)>c(OH-)=c(H+)
C.c(H+)+c(NH4+)=c(Cl-)+c(OH-)
D.c(H+)+c(Cl-)=c(NH4+)+c(NH3?H2O)+c(OH-)
参考答案:C
本题解析:
本题难度:简单
|