1、选择题 下列物质属于电解质的是(?)
A.金属钠
B.硫酸钠
C.干冰
D.石墨
参考答案:B
本题解析:溶液水或在熔融状态下能够导电的化合物是电解质,B正确,钠和石墨都是单质,不是电解质,也不是非电解质。干冰是CO2,属于非电解质,答案选B。
点评:判断电解质的关键不是看能否导电,关键是要看溶于水或在熔融状态下,能否电离出离子,能够自身电离出离子的化合物才是电解质,而导电只是一种现象。
本题难度:一般
2、选择题 食盐、蔗糖、醋酸、纯碱、汽油、明矾等是日常生活中经常使用的物质,下列有关说法或表示正确的是
[? ]
A.食盐溶于水形成的分散系,能发生丁达尔效应
B.蔗糖和醋酸都是弱电解质
C.纯碱是碱
D.明矾经水解可得到氢氧化铝胶体,1 L 0.2 mol/L的氢氧化铝胶体中含有氢氧化铝胶粒数小于0. 2NA
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列各项中,电离方程式正确的是
A.HCO3-+H2O CO32-+ H3O +
CO32-+ H3O +
B.H2SO3=2H++SO32-
C.NaHCO3 Na++HCO3-
Na++HCO3-
D.NaHSO4(熔融)=Na++H++ SO42-
参考答案:A
本题解析:H2SO3是弱电解质,部分电离,应为H2SO3 H++HSO3-、HSO3-
H++HSO3-、HSO3- H++SO32-,B错误;NaHCO3是强电解质,完全电离,应为NaHCO3=Na++HCO3-、HCO3-
H++SO32-,B错误;NaHCO3是强电解质,完全电离,应为NaHCO3=Na++HCO3-、HCO3- H++CO32-,C错误;熔融状态下共价键不断裂,硫酸氢钠熔融状态下电离方程式为NaHSO4(熔融)=Na++HSO4-,D错误。
H++CO32-,C错误;熔融状态下共价键不断裂,硫酸氢钠熔融状态下电离方程式为NaHSO4(熔融)=Na++HSO4-,D错误。
点评:强电解质完全电离、弱电解质部分电离、熔化状态共价键不断裂。
本题难度:一般
4、选择题 化学与生产生活密切相关,下列说法不正确的是( )
A.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
B.明矾和漂白粉常用于自来水的净化和杀菌消毒,其作用原理相同
C.合金材料钢铁在潮湿的空气中易发生电化学腐蚀
D.玻璃、陶瓷、水泥属于无机硅酸盐材料,其生产原料都需要石灰石
参考答案:A、血液属于胶体,不能透过半透膜,可利用渗析的方法分离胶体和溶液,血透的原理是利用渗析的方法净化血液,故A正确;
B、明矾净水的原理是铝离子水解生成的氢氧化铝具有净水作用,漂白粉的漂白原理是次氯酸的漂白性导致,二者常用于自来水的净化和杀菌消毒,其作用原理不相同,故B错误;
C、钢铁中的铁、碳和潮湿的空气构成原电池,铁为负极,易发生电化学腐蚀中的吸氧腐蚀,故C正确;
D、玻璃、陶瓷、水泥中主要成分是硅酸盐,均属于无机硅酸盐材料,其生产原料都需要石灰石,故D正确.
故选B.
本题解析:
本题难度:简单
5、填空题 (1)某温度(t℃)时,水的Kw=10-13,则该温度(填 “大于”“小于”或“等于”)____25℃,其理由是
___________________。将此温度下pH =11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
①若所得混合液为中性,则a:b___________
②若所得混合液的pH=2,则a:b___________
(2)某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA-;HA-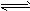 H++A2-
H++A2-
①Na2A溶液显____(填“酸性”“中性”或“碱性”),用一个等式表示0.1mol/L的Na2A溶液中所有离子间的关系___________;
②已知0.1mol/L NaHA溶液的pH =2,0.1 mol/L NaHA溶液中各种离子浓度由大到小的顺序是___________
参考答案:(1)大于;水的电离反应:H2O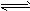 H++OH-是吸热反应,升温有利于水的电离,使Kw增大
H++OH-是吸热反应,升温有利于水的电离,使Kw增大
①10:1;②9:2
(2)①碱性;c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-);②c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
本题解析:
本题难度:一般