1、填空题 (1)石棉的主要成分为CaMg3Si4O12,把它写成氧化物的形式为______;
(2)质量相同的H2、NH3、Cl2、SO2、O3五种气体中,含有分子数目最多的是______,在相同温度和相同压强条件下,都为气体时体积最小的是______.
(3)请把硫酸在下列过程中所表现出的性质填写在空白处:
①浓硫酸常作某些气体的干燥剂:______;
②铜和浓硫酸加热,有气体放出:______;
③蔗糖中加入浓硫酸时,蔗糖变黑:______.
(4)元素周期表中位于第8纵行的铁元素属于第______族;表中最活泼的非金属元素位于第______纵行;目前元素周期表中所含元素为32种的周期是第______周期.
2、选择题 以下用于除去乙酸乙酯中乙酸和乙醇杂质的最好试剂是( )。
A.饱和碳酸钠溶液
B.氢氧化钠溶液
C.苯
D.水
3、填空题 硫酸是基础化学工业的重要的产品.它是许多化工生产的原料,大量用于制化肥,如磷肥、氮肥等.某化学兴趣小组围绕浓硫酸及其盐的性质进行如下探究,请你回答:
(1)将适量的蔗糖放入一烧杯中,再加入浓硫酸,观察到蔗糖变黑,体积膨胀,并产生刺激性气味的气体.该实验表明浓硫酸具有______.(填序号)
A.强酸性B.强氧化性C.脱水性D.吸水性
(2)取一小粒金属钠,小心放入盛有硫酸铜稀溶液的烧杯中,用漏斗倒扣在烧杯上,观察到金属钠在液面上四处游动,有大量气泡生成,收集产生的气体并点燃,火焰呈淡蓝色,该气体是______(填化学式).溶液中立即有蓝色沉淀生成,写出生成蓝色沉淀的离子方程式______.
(3)“绿色化学”要求综合考虑经济、技术、环保等方面来设计化学反应路线.若以铜为原料制取硫酸铜,通过以下两种方法均可以制得硫酸铜:
方法1:铜屑在空气中灼烧后,在加热条件下与稀硫酸反应.
方法2:铜与浓硫酸在加热条件下反应.请写出制取过程中发生反应的化学方程式.
方法1:______.方法2:______.
从原料利用率、环境保护等角度对比,应该选用哪种方法______.
(4)明矾KAl(SO4)2?12H2O是一种很好的净水剂,请用简要的文字描述其原理______.
4、选择题 下列材料中最不适宜制造储存浓硫酸的容器的是
A.铁
B.铝
C.铜
D.陶瓷
5、填空题 张明同学在学习“硫酸及其盐的某些性质与用途“中,进行如下实验探究.
[实验一]探究浓硫酸的氧化性
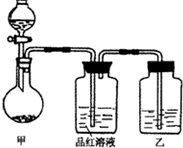
将实验室常用的药品放入如图所示的实验装置后,加热装置甲.(夹持和加热装置省略)
(1)该装置设计上存在明显缺陷,请指出:______.
(2)写出装置甲中反应的化学方程式:______.
(3)装置乙中的试剂是______.
[实验二]探究某硫酸亚铁盐固体是否变质
(4)请你帮助张明同学完成如下实验方案:
[实验三]用KHSO4制取H2O2并测其质量分数
查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,示意图如下:
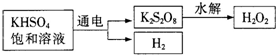
张明用此法制取一定浓度的H2O2,并进行下列实验测定H2O2的质量分数:(离子方程式:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑)
①取5.00mL?H2O2溶液(密度为1.00g/mL)置于锥形瓶中加水稀释,再加稀硫酸酸化;
②用0.1000mol/L?KMnO4溶液滴定;
③用同样方法滴定,三次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL.
回答下列问题:
(5)电解饱和KHSO4溶液时,阳极的电极反应式为______.
(6)操作②中,滴入第一滴KMnO4溶液,溶液紫红色消失很慢,随着滴定过程中Mn2+的增多,溶液紫红色消失速率加快.Mn2+的作用是______.
(7)原H2O2溶液中溶质的质量分数为______.