1、填空题 (1)石棉的主要成分为CaMg3Si4O12,把它写成氧化物的形式为______;
(2)质量相同的H2、NH3、Cl2、SO2、O3五种气体中,含有分子数目最多的是______,在相同温度和相同压强条件下,都为气体时体积最小的是______.
(3)请把硫酸在下列过程中所表现出的性质填写在空白处:
①浓硫酸常作某些气体的干燥剂:______;
②铜和浓硫酸加热,有气体放出:______;
③蔗糖中加入浓硫酸时,蔗糖变黑:______.
(4)元素周期表中位于第8纵行的铁元素属于第______族;表中最活泼的非金属元素位于第______纵行;目前元素周期表中所含元素为32种的周期是第______周期.
参考答案:(1)CaMg3Si4O12写成氧化物的形式为CaO?3MgO?4SiO2,故答案为:CaO?3MgO?4SiO2;
(2)n=mM=VVm=NNA可知,气体的摩尔质量越小,物质的量越多,分子数越多,体积越大,质量相同的H2、NH3、Cl2、SO2、O3五种气体中,氢气的摩尔质量最小,则分子数最多,氯气的摩尔质量最大,则物质的量最小,体积最小,
故答案为:H2、Cl2;
(3)①浓硫酸常作某些气体的干燥剂,利用了浓硫酸的吸水性,
铜和浓硫酸加热,有气体放出,为二氧化硫气体,同时生成硫酸铜,则利用了浓硫酸的强氧化性和酸性,
蔗糖中加入浓硫酸时,蔗糖变黑,利用了浓硫酸的脱水性,
故答案为:①吸水性;②强氧化性和酸性;③脱水性;
(4)铁位于周期表第Ⅷ族,周期表中最活泼的非金属元素位于第ⅦA族,位于第17列,目前元素周期表中所含元素为32种的周期是第六周期,含有镧系元素,
故答案为:Ⅷ;17;六.
本题解析:
本题难度:一般
2、选择题 以下用于除去乙酸乙酯中乙酸和乙醇杂质的最好试剂是( )。
A.饱和碳酸钠溶液
B.氢氧化钠溶液
C.苯
D.水
参考答案:A
本题解析:饱和碳酸钠溶液能溶解乙醇,也能吸收乙酸,同时可降低乙酸乙酯的溶解度。
本题难度:一般
3、填空题 硫酸是基础化学工业的重要的产品.它是许多化工生产的原料,大量用于制化肥,如磷肥、氮肥等.某化学兴趣小组围绕浓硫酸及其盐的性质进行如下探究,请你回答:
(1)将适量的蔗糖放入一烧杯中,再加入浓硫酸,观察到蔗糖变黑,体积膨胀,并产生刺激性气味的气体.该实验表明浓硫酸具有______.(填序号)
A.强酸性B.强氧化性C.脱水性D.吸水性
(2)取一小粒金属钠,小心放入盛有硫酸铜稀溶液的烧杯中,用漏斗倒扣在烧杯上,观察到金属钠在液面上四处游动,有大量气泡生成,收集产生的气体并点燃,火焰呈淡蓝色,该气体是______(填化学式).溶液中立即有蓝色沉淀生成,写出生成蓝色沉淀的离子方程式______.
(3)“绿色化学”要求综合考虑经济、技术、环保等方面来设计化学反应路线.若以铜为原料制取硫酸铜,通过以下两种方法均可以制得硫酸铜:
方法1:铜屑在空气中灼烧后,在加热条件下与稀硫酸反应.
方法2:铜与浓硫酸在加热条件下反应.请写出制取过程中发生反应的化学方程式.
方法1:______.方法2:______.
从原料利用率、环境保护等角度对比,应该选用哪种方法______.
(4)明矾KAl(SO4)2?12H2O是一种很好的净水剂,请用简要的文字描述其原理______.
参考答案:(1)蔗糖逐渐变黑表现了浓硫酸的脱水性,放出有刺激性气味的气体说明浓硫酸具有强氧化性;
故答案为:BC.
(2)钠在硫酸铜溶液中先和水反应生成氢氧化钠和氢气,2Na+2H2O=2NaOH+H2↑,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,生成的气体为氢气,生成的蓝色沉淀为氢氧化铜沉淀,反应的离子方程式为:Cu2++2OH-=Cu(OH)2↓;
故答案为:H2,Cu2++2OH-=Cu(OH)2↓;
(3)方法1、铜屑在空气中灼烧后生成氧化铜,氧化铜在加热条件下与稀硫酸反应生成硫酸铜和水,反应的化学方程式为:2Cu+O2+2H2SO4=2CuSO4+2H2O;
方法2、铜和浓硫酸反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)△.CuSO4+SO2↑+2H2O;
相同质量的硫酸生成硫酸铜方法1多,且无污染性气体,方法2反应过程中有二氧化硫污染性的气体生成,消耗同质量硫酸生成的硫酸铜少;
故答案为:2Cu+O2+2H2SO4=2CuSO4+2H2O,Cu+2H2SO4(浓)△.CuSO4+SO2↑+2H2O;方法1;
(4)明矾溶解于水中,溶液中铝离子水解生成氢氧化铝胶体具有吸附悬浮在水中的杂质的作用,明矾溶于水后溶液中的铝离子水解生成氢氧化铝胶体,胶体具有吸附悬浮杂质的作用,起到净水的作用;
故答案为:明矾溶于水后溶液中的铝离子水解生成氢氧化铝胶体,胶体具有吸附悬浮杂质的作用,起到净水的作用;
本题解析:
本题难度:一般
4、选择题 下列材料中最不适宜制造储存浓硫酸的容器的是
A.铁
B.铝
C.铜
D.陶瓷
参考答案:C
本题解析:铁、铝在冷的浓硫酸中发生钝化,陶瓷与浓硫酸不反应。铜能与浓硫酸反应,不能用铜为原料制造储存浓硫酸的容器。
本题难度:一般
5、填空题 张明同学在学习“硫酸及其盐的某些性质与用途“中,进行如下实验探究.
[实验一]探究浓硫酸的氧化性
将实验室常用的药品放入如图所示的实验装置后,加热装置甲.(夹持和加热装置省略)
(1)该装置设计上存在明显缺陷,请指出:______.
(2)写出装置甲中反应的化学方程式:______.
(3)装置乙中的试剂是______.
[实验二]探究某硫酸亚铁盐固体是否变质
(4)请你帮助张明同学完成如下实验方案:
[实验三]用KHSO4制取H2O2并测其质量分数
查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,示意图如下:
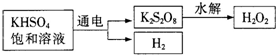
张明用此法制取一定浓度的H2O2,并进行下列实验测定H2O2的质量分数:(离子方程式:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑)
①取5.00mL?H2O2溶液(密度为1.00g/mL)置于锥形瓶中加水稀释,再加稀硫酸酸化;
②用0.1000mol/L?KMnO4溶液滴定;
③用同样方法滴定,三次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL.
回答下列问题:
(5)电解饱和KHSO4溶液时,阳极的电极反应式为______.
(6)操作②中,滴入第一滴KMnO4溶液,溶液紫红色消失很慢,随着滴定过程中Mn2+的增多,溶液紫红色消失速率加快.Mn2+的作用是______.
(7)原H2O2溶液中溶质的质量分数为______.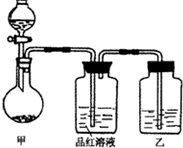
参考答案:(1)装置乙是用于吸收二氧化硫气体,所以没有必要有瓶塞;故答案为:装置乙不应有瓶塞;
(2)铜和浓硫酸反应生成硫酸铜、二氧化硫和水,反应的化学方程式:Cu+2H2SO4(浓)?△?.?CuSO4+SO2↑+2H2O(或C+2H2SO4(浓)?△?.?CO2↑+2SO2↑+2H2O);
故答案为:Cu+2H2SO4(浓)?△?.?CuSO4+SO2↑+2H2O(或C+2H2SO4(浓)?△?.?CO2↑+2SO2↑+2H2O);
(3)二氧化硫属于酸性氧化物,可用碱液吸收;故答案为:氢氧化钠溶液(或氢氧化钾溶液等);
(4)亚铁离子易很容易被氧化为三价铁离子,可以用硫氰酸钾来检验,即三价铁离子往一支试管中加入少量固体,加水溶解,再滴加几滴KSCN溶液;若溶液变为红色,说明该固体已变质,若溶液未变红色,说明该固体没有变质,
故答案为:三价铁离子往一支试管中加入少量固体,加水溶解,再滴加几滴KSCN溶液;若溶液变为红色,说明该固体已变质,若溶液未变红色,说明该固体没有变质;
(5)电解饱和KHSO4溶液时,阳极是阴离子发生失电子的氧化反应,电极反应式为2HSO4--2e-=S2O82-+2H+
(或2SO42--2e-=S2O82-),故答案为:2HSO4--2e-=S2O82-+2H+(或2SO42--2e-=S2O82-);
(6)在双氧水的分解过程中,高锰酸钾具有氧化性,对应的还原产物是锰离子,当加入第一滴KMnO4溶液,溶液紫红色消失很慢,随着滴定过程中Mn2+的增多,溶液紫红色消失速率加快,可见是锰离子起到催化剂的作用,
故答案为:催化剂(或加快反应速率);
(7)三次消耗KMnO4溶液的体积分别为20.00mL、19.98mL、20.02mL,则体积平均值为:20.00mL,则消耗高锰酸根的量:0.1mol/L×0.02L=0.002mol,设双氧水的物质的量为n,则
2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑
2? 5
0.002mol n
解得n=0.005mol,所以双氧水的质量为:0.005mol×34g/mol=0.17g,双氧水的质量分数=0.17g5.00mL×1.00g/mL×100%=3.4%,故答案为:3.4%.
本题解析:
本题难度:一般