| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ���ʵ�������Ƶ������ѵ��2019�����°棩(ʮ)
�ο��𰸣�B ��������� �����Ѷȣ��� 2��ѡ���� NA���������ӵ�����������˵����ȷ���� �� �� |
�ο��𰸣�B
�����������
�����Ѷȣ���
3��ѡ���� ij�¶��£�V?mL������NaNO3��Һa?g��������b?gˮ�����b?g?NaNO3����(�ָ���ԭ�¶�)����ʹ��Һ�ﵽ���ͣ����������ļ�������ȷ����
[? ]
A�����¶���NaNO3���ܽ��Ϊ100?g
B��ԭ��������Һ��NaNO3����������Ϊ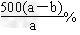
C��ԭ��������Һ��NaNO3�����ʵ���Ũ��Ϊ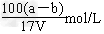
D��ԭ��������Һ���ܶ�Ϊ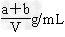
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
4��ѡ���� ������Һ���й����ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�������
A��pH��ȵ�CH3COONa��NaOH��Na2CO3������Һ��[NaOH]��[CH3COONa]��[Na2CO3]
B��Na2CO3��Һ��[Na+]��[CO32-]֮��Ϊ2��1
C��[NH4+]��ȵ�NH4Cl��NH4HCO3��NH4HSO4������Һ��[NH4HSO4]��[NH4Cl]��[NH4HCO3]
D����֭������ѪҺ��������Һ��θҺ��[H+]���ν���
�ο��𰸣�A��ǿ�������Σ���Ӧ�������Խ����ˮ��̶�Խ����Һ�����ʵ����ʵ���ԽС�����Դ�С��ϵΪ�����̼�ᣬ����̼����ˮ��̶ȴ�pH��ͬʱ�������Ƶ�Ũ�ȴ���̼���Ƶ�Ũ�ȣ���������Ϊǿ�Ũ����С������pH��ͬ������Ũ�ȹ�ϵΪ��[NaOH]��[Na2CO3]��[CH3COONa]����A����
B��̼������Һ�У�����̼������ӷ�����ˮ�⣬���ʵ�����С������[Na+]��[CO32-]֮�ȴ���2��1����B����
C���Ȼ���������������Ρ�̼������������������Σ�����˫ˮ�⣬ˮ��̶�����̼�������Һ��ʾ���ԣ���Һ�е������������������ˮ�⣬������Һ�������Ũ����ȣ�������ҺŨ�����㣺��[NH4HSO4]��[NH4Cl]��[NH4HCO3]����C��ȷ��
D��ѪҺ��7.35��7.45��θҺ��0.9��1.5����֭��ʾ�����ԣ�pH��3.5���ҡ����dz����ԣ�����������Ũ��Ϊ��θҺ����֭�����ǣ�ѪҺ����D����
��ѡC��
���������
�����Ѷȣ���
5��ѡ���� ����˵������ȷ���ǡ�(����)
A��1 Lˮ���ܽ���58��5 g NaCl������Һ�����ʵ���Ũ��Ϊ1 mol��L-1
B����1 L 2 mol��L-1��H2SO4��Һ��ȡ��0��5 L������Һ��Ũ��Ϊ1 mol��L-1
C������500 mL 0��5 mol��L-1��CuSO4��Һ����62��5 g����
D���к�100 mL 1 mol��L-1��H2SO4��Һ����NaOH 4 g
�ο��𰸣�C
��������� A��58��5 g NaCl����1 Lˮ��������Һ�����������1 L����Ũ�Ȳ���1 mol��L-1��B��ȡ���IJ�����ҺŨ����Ϊ2 mol��L-1��D���к�100 mL
1 mol��L-1��H2SO4��Һ����0��2 mol NaOH������Ϊ8 g��
���㣺��Һ�����Ƽ�����
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���ܽᡶ���ʵ�����.. | |
| �����Ŀ |