1、选择题 下列实验操作错误的是
A.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C.浓H2SO4稀释时,应将浓H2SO4慢慢加到H2O中,并及时搅拌和冷却
D.用酒精萃取碘水中的碘
参考答案:D
本题解析:酒精和水是互溶的,因此不能用作萃取碘水中碘的萃取剂,应该用苯或四氯化碳,选项D不正确,其余都是正确的,答案选D。
本题难度:一般
2、选择题 某溶液中含有Cl-、SO42-、Fe3+、K+、M,且离子物质的量之比为2:3:1:3:2,则微粒M可能为
A.Na+
B.Ag+
C.Ba2+
D.Mg2+
参考答案:A
本题解析:分析:某溶液中含有Cl-、SO42-、Fe3+、K+、M,,溶液不显电性,利用电荷守恒及离子的共存来计算解答.
解答:溶液中含有Cl-、SO42-、Fe3+、K+、M,且离子物质的量之比为2:3:1:3:2,
设M的电荷为x,
由电荷守恒可知,
2×1+3×2=1×3+3×1+x×2,
解得x=+1,
则C、D选项排除,又Ag+与Cl-、SO42-不能共存,
则M可能为Na+,
故选A.
点评:题考查物质的量的有关计算,明确电荷守恒、离子的共存是解答本题的关键,选项B为易错点,题目难度不大.
本题难度:简单
3、选择题 标准状况下,1 mL的水溶解350 mL的氨气,所得氨水的密度为0.9 g・mL-1,则氨水的物质的量浓度为(单位:mol・L-1)
A.0.15
B.52.8
C.25.6
D.11.12
参考答案:D
本题解析:根据题目条件设取了1 mL水,所以氨气的物质的量为0.35/22.4 mol,氨水的体积为[(1+0.35/22.4×17)÷0.9]mL,所以所得氨水的物质的量浓度为11.12 mol・L-1.
本题难度:一般
4、实验题 某固体混合物可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
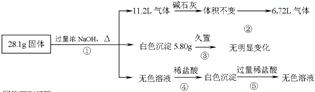
回答下列问题:
(1)混合物中是否存在FeCl2?___(填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4?___(填“是”或“否”),你的判断依据是?。
(3)写出反应④的离子反应式:?__?。
(4)请根据计算结果判断混合物中是否含有AlCl3(说出你的计算依据,不要求写计算过程)
?。
(5)把AlCl3溶液中加热浓缩蒸干,不能得到AlCl3・6H2O晶体,请你设计一个可行的简易实验方案,怎样从溶液中得到较纯的AlCl3・6H2O晶体。
?
?。
参考答案:(1)否;(2)是,气体通过浓硫酸减少4.48L。
(3) AlO2-+H++H2O ==Al(OH)3↓。
(4)由题中信息可推得一定含有Al、(NH4)2SO4和MgCl2三种物质,而计算出这三种物质的质量之和刚好等于28.1g,所以一定没有AlCl3。
(5)往氯化铝溶液中加入一定量的浓盐酸,蒸发浓缩,降温结晶,过滤。
本题解析:略
本题难度:简单
5、选择题 如果你家里的食用花生油混有水分,你将采取下列何种方法分离
[? ]
A.过滤
B.蒸馏
C.分液
D.萃取
参考答案:C
本题解析:
本题难度:简单