1、计算题 “温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组
| 温度/℃
| 起始量/mol
| 平衡量/mol
| 达到平衡所需时间/min
|
CO
| H2O
| H2
| CO
|
1
| 650
| 4
| 2
| 1.6
| 2.4
| 6
|
2
| 900
| 2
| 1
| 0.4
| 1.6
| 3
|
3
| 900
| a
| b
| c
| d
| t
|
?
① 实验1条件下平衡常数K=?(保留小数点后二位数字)。
② 实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值?(填具体值或取值范围)。
③ 实验4,若900℃时,在此容器中加入10molCO、5molH2O、2molCO2、5molH2,则此时v(正)?v(逆)(填“<”、“>”、“=”)。
(2)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10―9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10―4mo1/L,则生成沉淀所需CaCl2溶液的最小浓度为?。
(3)已知BaSO4(s) + 4C(s) ="4CO(g)" + BaS(s)?△H1 =+571.2kJ/mol,
BaSO4(s) + 2C(s) = 2CO2(g) + BaS(s)?△H2="+226.2" kJ/mol。
则反应C(s) + CO2(g) = 2CO(g)的△H3=?kJ/mol。
 (4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li ?LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为:??和?。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为?。(Li的相对原子质量约为7.0)
(4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li ?LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为:??和?。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为?。(Li的相对原子质量约为7.0)
2、选择题 在密闭容器中存在下列平衡:CO(g)+H2O(g)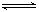 CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g),CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
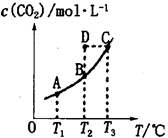
A.平衡状态A与C相比,平衡状态A的c(CO)小
B.在T2时,若反应处于状态D,则一定有v正<v逆
C.反应CO(g)+H2O(g)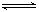 CO2(g)+H2(g)△H>0
CO2(g)+H2(g)△H>0
D.若T1、T2时的平衡常数分别为K1、K2,则K1<K2
3、选择题 某温度下,将2mo1A和3mo1B充入一密闭容器中,发生反应:aA(g)+B(g)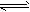 C(g)+D(g),5min 后达到平衡。已知该温度下其平衡常数K=1 ,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则
C(g)+D(g),5min 后达到平衡。已知该温度下其平衡常数K=1 ,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则
[? ]
A.a=1
B.a=2
C.B的转化率为40%
D.B的转化率为60%
4、选择题 已知A(s)+2B(g)  2C(g)+D(g)?△H<0 在一密闭容器中反应的υ-t图。t1时,改变了一个条件,下列叙述正确的是
2C(g)+D(g)?△H<0 在一密闭容器中反应的υ-t图。t1时,改变了一个条件,下列叙述正确的是
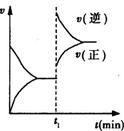
A.t1时,一定是升高了反应的温度
B.t1时,可能是向容器中通入了一定量的C气体
C.t1时,可能是向容器中加入了催化剂
D.t1时改变外界条件后,该反应的平衡常数可能减小,也可能不变
5、选择题 已知300℃、70MPa下由二氧化碳和氢气合成乙醇的反应成为现实:
2CO2(g)+6H2(g) ?CH3CH2OH(g)+3H2O(g)。在温度为T℃,容积不变的密闭容器中,将3molH2和1molCO2混合,达到平衡时乙醇气体的体积分数为a,下列有关说法正确的是
?CH3CH2OH(g)+3H2O(g)。在温度为T℃,容积不变的密闭容器中,将3molH2和1molCO2混合,达到平衡时乙醇气体的体积分数为a,下列有关说法正确的是
A.升高温度,该反应的平衡常数将增大
B.再向该容器中充入1molH2和1molCO2,达到平衡时,H2的转化率将高于CO2
C.加入催化剂或从平衡混合气中分离出水蒸气均可提高CO2和H2的利用率
D.T℃,在容积可变的密闭容器中将3molH2和1molCO2混合,达到平衡时乙醇的体积分