1、实验题 某同学设计的制取氯气和验证氯气部分化学性质的实验装置如下图所示:
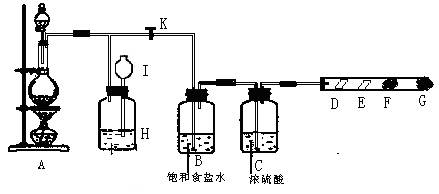 其中D处放有干燥的紫色石蕊试纸,E处放有湿润的紫色石蕊试纸, F、G处依次放有喷上少量淀粉KI溶液、浓NaOH溶液的棉球。回答下列问题:
其中D处放有干燥的紫色石蕊试纸,E处放有湿润的紫色石蕊试纸, F、G处依次放有喷上少量淀粉KI溶液、浓NaOH溶液的棉球。回答下列问题:
(1)在装置A中放入有关药品后,打开活塞K,将分液漏斗中的液体加入烧瓶中,关闭分液漏斗的活塞,点燃酒精灯,请写出A处反应的化学方程式:?
(2)B处饱和食盐水是为了除去?。
(3)在E处,紫色石蕊纸的颜色由紫色变为红色,再变为无色,其原因是?
?。
(4)当F处棉球变色,立即关闭活塞K,可看到I瓶中液面上升,H瓶中充满黄绿色气体。
则甲装置的作用为?。
(5)G处可能发生反应的化学方程式?。
2、填空题 同温同压下,相同体积的SO2和H2S气体的分子数之比是_______,质量之比是_______,密度之比是________。两种气体等体积混合后的平均摩尔质量是________,该混合气体对氢气的相对密度是______。同温同压下,相同质量的SO2和H2S气体的分子数之比是________,体积之比是_________,所含原子数之比______。
3、选择题 NA表示阿伏伽德罗常数的值,下列叙述中不正确的是
A.分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
4、填空题 NH3的摩尔质量为________,一个NH3分子的质量是________(用含NA的式子表示),1.204×1024个NH3
分子物质的量为__________,所含电子的物质的量为__________,共含________个氢原子。同温同压下相同体积的NH3和H2S分子数之比为__________,原子数之比为__________,质量之比为__________。
5、选择题 同温同压下,同体积的气体单质X2和气体单质Y2化合生成Z,其体积不变,则Z的化学式为( )
A.X2Y2
B.X2Y
C.XY2
D.XY