1������� ����ת����ϵͼ�У�A��B��C��D��E������Ϊ���壬B��E��F��KΪ���ʣ�����FΪ��ɫ���壻C��D����ʹ�����ʯ��ˮ����ǣ�D��E����ʹƷ����Һ��ɫ��I��һ�ֺ���ɫ�����������ش��������⣺
��1��E�ĵ���ʽΪ______��
��2����Ӧ�۵����ӷ���ʽΪ______��
��3��F��G����Һ��Ӧ�Ļ�ѧ����ʽΪ______��
��4��������ҺL�н��������ӵķ�����______��
��5������A���ܶ�Ϊ��ͬ״���������ܶȵ�30������A�к�3�����Ԫ�أ�ͨ�����㡢��������ȷ��A�ķ���ʽΪ______���˷���ʽ��Ԫ�ط�����д����������Ԫ��ԭ����������С�С�˳�����У���A�����и�ԭ�Ӿ���8�����ȶ��ṹ������ṹʽΪ______��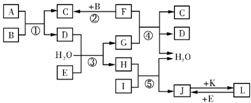
�ο��𰸣�C��D����ʹ�����ʯ��ˮ����ǣ���ʹ����ʯ��ˮ����ǵ������ж�����̼�Ͷ�����������C��D���ڶ�����̼�Ͷ�������EΪ���ʣ�D��E����ʹƷ����Һ��ɫ����ʹƷ����Һ��ɫ���������Ͷ�����������D�Ƕ�������C�Ƕ�����̼��E��������I��һ�ֺ���ɫ���������I����������B��FΪ���ʣ�����FΪ��ɫ���壬F��B��Ӧ���ɶ�����̼������F��̼��B��������A��������Ӧ���ɶ�����̼�Ͷ�����������A�ǣ�������ˮ����������Ӧ������������ᣬ̼�����ᷴӦ������G�����ᣬH������������������Ӧ�����Ȼ�����ˮ������J���Ȼ�����KΪ���ʣ�J��K��Ӧ����L��L��������Ӧ�����Ȼ���������L���Ȼ�������K������
��1��E��������E�ĵ���ʽΪ��
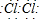
��
�ʴ�Ϊ��
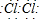
��
��2�������Ͷ�������ˮ��Ӧ������������ᣬ���ӷ�Ӧ����ʽΪ��Cl2+SO2+2H2O=2Cl-+SO42-+4H+��
�ʴ�Ϊ��Cl2+SO2+2H2O=2Cl-+SO42-+4H+
��3��̼�������ڼ��������·�Ӧ���ɶ�������Ͷ�����̼��ˮ��
��Ӧ����ʽΪ��C+2H2SO4��Ũ��?��?.?CO2��+2SO2��+2H2O��
�ʴ�Ϊ��C+2H2SO4��Ũ��?��?.?CO2��+2SO2��+2H2O��
��4�����������ӵļ��鷽���ǣ�����Һ�еμ�KSCN��Һ����Һ����ɺ�ɫ���μ���ˮ����Һ���ɫ��֤���ж��������Ӵ��ڣ�
�ʴ�Ϊ������Һ�еμ�KSCN��Һ����Һ����ɺ�ɫ���μ���ˮ����Һ���ɫ��
��5������A���ܶ�Ϊ��ͬ״���������ܶȵ�30��������A����Է�������������30������A����Է�����Ϊ60����A�к�3�����Ԫ�أ�ͨ�����Ϸ���A��һ���������̼Ԫ�أ���A��������Ӧ�����ɶ�������Ͷ�����̼������A������Ԫ�أ�����ʽΪSCO��A�����и�ԭ�Ӿ���8�����ȶ��ṹ������ṹʽΪS=C=O��
�ʴ�Ϊ��SCO��S=C=O��
���������
�����Ѷȣ�һ��
2������� ��6�֣���ͼ��һЩ�����ĵ��ʡ�������֮���ת����ϵͼ����Щ��Ӧ�еIJ������ʱ���ȥ����Ӧ�ٳ���Ӧ����Ұ�⺸�Ӹֹ죬AΪ�ճ������г����Ľ������ʣ� GΪ����ɫ���壬F�Ǻ�ˮ�к����ε���Ҫ�ɷ֣�JΪD��G��Ӧ�����γɵ�ˮ��Һ��

��ش��������⣺
��1��H�Ļ�ѧʽΪ_______________����2����Ӧ���ڹ�ҵ��ͨ����֮Ϊ__________��ҵ��
��3��д����Ӧ�۵����ӷ���ʽ?��
��4��д����Ӧ�ڵĻ�ѧ����ʽ?��
�ο��𰸣���6�֣�(1)NaOH? (2)�ȼҵ
��3��Al2O3+2OH- =2AlO2-+H2O? 2NaCl+2H2O=2NaOH+H2+Cl2
�����������
�����Ѷȣ�һ��
3������� (10��)����ͼ��ʾ�ķ�Ӧ��ϵ��A����ѧ���������A��B��C�к���ͬһ��Ԫ��R������R��Ԫ���Ѿ���ȥ��
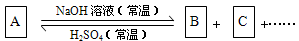
(1)��A��NaOH����ͬ���ʵ����ȷ�Ӧ���ȿ�ֻ����B���ֿ�ֻ����C����������B+C��
��д������������Ӧ��ϵ��A�Ļ�ѧʽ?��
��д�������йط�Ӧ�����ӷ���ʽ��
����B�����ӷ���ʽΪ?��
����C�����ӷ���ʽΪ?��
��2����A��NaOH�����Ժ������ʵ����ȷ�Ӧ��������ΪB+C����A�ķ���ʽ������
?��ֻдһ�֣����÷�Ӧ�����ӷ���ʽΪ?��
R��A��B��C�еĻ��ϼ۱��������������?��
�ο��𰸣���10�֣�
CO2����AlCl3����? CO2+2OH-=CO32-+H2O��? CO2+OH-=HCO3-��
Cl2+2OH-=Cl-+ClO-+H2O��? R��A�еĻ��ϼ۴���B��C�л��ϼ�֮�䣻
�����������
�����Ѷȣ���
4��ѡ���� ��֪�ס��ҡ������������������ԭ������Ϊǰ18�ŵ�Ԫ����ɣ�������֮���ת����ϵ���£�
��
������������˵����ȷ���ǣ�������
A����һ��Ϊ����
B����һ��Ϊ������
C����һ��Ϊ��
D���ס��ҡ�����������Է�������һ����16��16�ı���
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5������� ���и������뻯����֮��Ĺ�ϵ��ͼ�����ʼ�����������Ԫ�ؽ�Ϊ������Ԫ�أ�
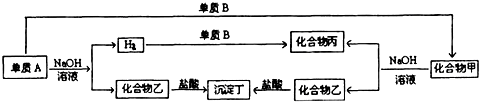
��1���������������ڹ��������ᣬ����AΪ______��Ϊ______��
�����������ڹ��������ᣬ����AΪ______��Ϊ______��
��2���ٳ����������ڹ�������ʱ���������������ᷴӦ��______��
�ڳ��������ڹ�������ʱ������������������ᷴӦ��______��
�ο��𰸣���1�����ת����ϵ��֪���������������ڹ��������ᣬ��ΪH2SiO3����AΪSi�������������ڹ��������ᣬ����ת����ϵ��֪����ΪAl��OH��3����AΪAl������B��Ӧ���ɼף����ܺ�����������Һ��Ӧ���������ܺ�����������Һ��Ӧ������B������������Al2O3��
�ʴ�Ϊ��Si��H2SiO3��Al��Al2O3��
��2���ٳ����������ڹ�������ʱ���������������ᷴӦΪNa2SiO3+2HCl�TH2SiO3��+2NaCl���ʴ�Ϊ��Na2SiO3+2HCl�TH2SiO3��+2NaCl��
�ڳ��������ڹ�������ʱ������������������ᷴӦΪNaAlO2+HCl+H2O�TAl��0H��3��+NaCl���ʴ�Ϊ��NaAlO2+HCl+H2O�TAl��0H��3��+NaCl��
���������
�����Ѷȣ�һ��