1、选择题 化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
[? ]
A.CO2的电子式 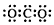
B.Cl-的结构示意图 
C.乙烯的结构简式 C2H4
D.质量数为37的氯原子 1737Cl
参考答案:B
本题解析:
本题难度:简单
2、简答题 中学课堂实验提到,让蒸馏水通过酸式滴定管如线状慢慢流下,把摩擦带电的玻璃棒靠近水流,发现水流的方向发生偏转。问:如果把盛在玻璃容器中的蒸馏水置于强磁场的两极之间,蒸馏水的体积是增大、缩小还是保持不变?其原因是什么?
__________________________________
参考答案:体积增大。由于水是极性分子,置于强磁场中时,水分子在一定程度上被强迫做定向排列,导致部分水分子之间相互以同一电(磁)极相斥,产生斥力,体积因此而增大。
本题解析:
本题难度:一般
3、选择题 某元素最高正价与负价绝对值之差为4,该元素的离子跟与其核外电子排布相同的离子形成的化合物是
[? ]
A.K2S
B.MgS
C.MgO
D.NaF
参考答案:A
本题解析:
本题难度:简单
4、选择题 下列生活中的问题,不能用金属键的知识解释的是
[? ]
A.用铁制品做炊具
B.用金属铝制成导线
C.用铂金做首饰
D.铁易生锈
参考答案:D
本题解析:
本题难度:简单
5、填空题 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比
B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为序40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子的数目之比为2∶1。请回答下列问题。
(1)A单质、B单质、化合物R的熔点大小顺为下列的________(填序号)。
①A单质>B单质>R? ②R>A单质>B单质
③B单质>R>A单质? ④A单质>R>B单质
(2)CB3分子的空间构型是________,其固体时的晶体类型为______________。
(3)写出D原子的核外电子排布式:________________________,C的氢化物比D的氢化物在水中的溶解度大得多的原因是__________________________________________。
(4)B元素和D元素的电负性大小关系为____________。
(5)A与B形成的离子化合物的晶胞中,每个A+周围与它距离相等且最近的B-有______个,这些B-围成的空间几何构型为____________。
参考答案:(8分每空一分)? (1)②? (2)三角锥形 分子晶体
(3)1s22s22p63s23p4 NH3与水分子之间可以形成氢键且发生化学反应
(4)B>D (5)6 正八面体
本题解析:B原子得一个电子后3p轨道全满,则B应该是氯元素。又因为A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,所以A是钠元素。C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大,所以C是氮元素。D的最高化合价和最低化合价的代数和为4,则D是第ⅥA族元素。最高价氧化物中含D的质量分数为40%,则有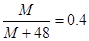 。即M=32。由于且其核内质子数等于中子数,所以D是16号元素S元素。R是由A、D两元素形成的离子化合物,其中A与D离子的数目之比为2∶1,则R是硫化钠。
。即M=32。由于且其核内质子数等于中子数,所以D是16号元素S元素。R是由A、D两元素形成的离子化合物,其中A与D离子的数目之比为2∶1,则R是硫化钠。
(1)钠是金属晶体,氯气形成的晶体是分子晶体,硫化钠形成的晶体是离子晶体,则A单质、B单质、化合物R的熔点大小顺为R>A单质>B单质,答案选②。
(2)氨气是三角锥形结构,形成的晶体是分子晶体。
(3)根据构造原理可知,S原子的核外电子排布式是1s22s22p63s23p4。由于NH3与水分子之间可以形成氢键且发生化学反应,所以氨气的溶解性大于H2S的溶解性。
(4)非金属性越强,电负性越大,所以氯元素的电负性大于S元素的电负性。
(5)根据氯化钠的晶胞结构特点可知,每个A+周围与它距离相等且最近的B-有6个,这些B-围成的空间几何构型为正八面体。
点评:该题是高考中的常见题型,试题综合性强,贴近高考,试题注重基础,侧重能力的培养和训练,有利于培养学生的逻辑推理能力和抽象思维能力。该题主要是以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:困难