1、选择题 下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)( )
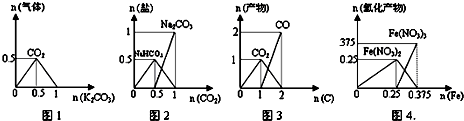
A.图1:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体
B.图2:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐
C.图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物
D.图4:n(HNO3)=1mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO)
参考答案:C
本题解析:
本题难度:简单
2、选择题 对于下列各组中的两种物质,取等物质的量分别在足量氧气中燃烧,耗氧量相同的是( )
A.乙醇和乙酸
B.葡萄糖和环己烷
C.丙烷和乙酸乙酯
D.乙醛和乙醇
参考答案:CxHyOz+(x+y4-z2)O2点燃
本题解析:
本题难度:一般
3、选择题 需要加入氧化剂才能实现的变化是
A.MnO2→MnSO4
B.AlCl3→Al(OH)3
C.KI→KIO3
D.HNO3→NO
参考答案:C
本题解析:需要加入氧化剂才能实现,说明该物质具有还原性,在反应中化合价要升高。符合条件的为C,所以选C。
本题难度:简单
4、填空题 Ⅰ.按要求填空(每空1分)
①KOH的电子式:??②NH4Cl的电子式:??
③CO2的结构式:????④HClO的结构式: ?
Ⅱ.按要求填空(每空2分)
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa(25℃时)时,已知0.5mol液态肼与足量氧气反应,生成氮气和水蒸气,放出312 KJ的热量。N2H4完全燃烧反应的热化学方程式是?;又已知H2O(l)==H2O(g);△H = +44kJ?mol-1,由64g液态肼与氧气反应生成液态水时放出的热量是?kJ。
参考答案:Ⅰ.①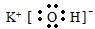 ?②
?②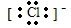
③? O=C=O?④H-O-Cl? (各1分)
Ⅱ.N2H4(1)+O2(g)=N2(g)+2H2O(g)△H=-624kJ/mol(2分)(出现错误扣2分)1424(2分)
本题解析:Ⅰ.①氢氧化钾是离子化合物,其电子式应采用离子化合物的书写形式,答案为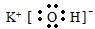 ,
,
②氯化铵也是离子化合物,但阳离子的电子式不是其离子符号,答案为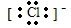 ;
;
③CO2分子中C与O以2对共用电子对结合,所以结构式为O=C=O;
④HClO分子中O分别与H、Cl原子形成共价单键,结构式为H-O-Cl;
Ⅱ.0.5mol液态肼与足量氧气反应,生成氮气和水蒸气,放出312 KJ的热量。则1mol肼完全燃烧放出624KJ的热量,热化学方程式为N2H4(1)+O2(g)=N2(g)+2H2O(g)△H=-624kJ/mol;水蒸气生成液态水放出热量,64g肼的物质的量是2mol,所以放出的热量是2×624kJ+4×44 kJ=1424kJ。
本题难度:一般
5、选择题 若M2O7x-+3S2-+14H+=2M3++3S↓+7H2O,则M2O7x-中的M的化合价为
A.+2
B.+3
C.+4
D.+6