1、选择题 已建立化学平衡的某可逆反应,当改变反应条件使化学平衡向正反应方向移动时,下列叙述正确的是
[? ]
①生成物的体积分数一定增加 ②生成物的产量一定增加
③反应物的转化率一定增大 ④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率 ⑥使用了合适的催化剂
A.①②
B.②⑤
C.③⑤
D.④⑥
参考答案:B
本题解析:
本题难度:一般
2、选择题 如图I所示,甲、乙之间的隔板K和活塞F都可以左右移动,甲中充入2 molA和l mol B,乙中充入2mol C和1 mol He,此时K停在0处。在一定条件下发生反应:2A(g)+ B(g)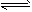 2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是
2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是

[? ]
A. 达到平衡时,隔板K最终停留在刻度0与-2之间
B. 若达到平衡时,隔板K最终停留在刻度-1处,则乙中C的转化率小于50%
C. 若达到平衡时,隔板K最终停留在靠近刻度-2处,则乙中F最终停留刻度大于4
D. 若图I中x轴表示时间,则y轴可表示甲、乙两容器中气体的总物质的量或A 的物质的量
参考答案:AC
本题解析:
本题难度:一般
3、选择题 可逆反应mA(固)+ nB(气)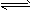 eC(气)+fD(气)反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度(T)和不同压强(p)的条件不随时间(t)的变化关系如图所示。下列叙述正确的是
eC(气)+fD(气)反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度(T)和不同压强(p)的条件不随时间(t)的变化关系如图所示。下列叙述正确的是
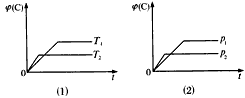
[? ]
A.达到平衡后,若使用催化剂,C的体积分数将增大
B.达到平衡后,若温度升高,化学平衡向逆反应方向移动
C.化学方程式中,n>e+f
D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
参考答案:B
本题解析:
本题难度:一般
4、填空题 一碳化学是指以研究分子中只含一个碳原子的化合物[如甲烷(CH4)、合成气(CO和H2)、CO2、CH3OH等]为原料来合成一系列化工原料和燃料的化学。科学家提出一种“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为其它化工原料,如下图所示。
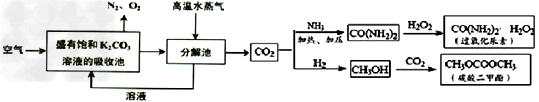
(1)碳酸钾溶液所起的作用是__________。
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)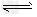 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
①?下图表示该反应过程中能量(单位为kJ/mol)的变化,关于该反应的下列说法中,正确的是__________?(填字母)。?
A.△H>0,△S>0?B.△H>0,△S<0
C.△H<0,△S<0?D.△H<0,△S>0
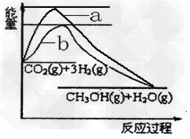
在上图中,曲线_______?(填:a或b)表示使用了催化剂。
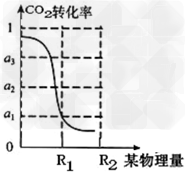
②?在压强为5MPa,体积为VL的反应室中,bmolCO2与?3bmolH2在催化剂作用下反应生成甲醇,CO2的转化率与某物理量的关系如下图。则表中横坐标的物理量为__________,R1时该反应的平衡常数K=________________(用含字母的代数式表示)。当该物理量从R1到?R2进行?改变,平衡常数K将________(填“增大”、“不变”或“减小”)。
(3)过氧化尿素合成反应式如下:CO(NH2)2?+H2O2?→?CO(NH2)2・H2O2?△H<0。当n?(过氧化氢):n?(尿素)?为?1.3∶1,反应时间45?min,用水杨酸作为稳定剂,分别考察反应温度对反应效果的影响如下图所示(活性氧含量可视为CO(NH2)2・H2O2产量的直观表示)
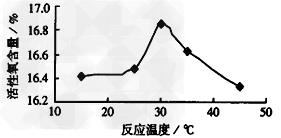
从图中可以看出,在实验选定的温度范围内,随反应温度的升高,产品活性氧含量先增加而随后减少。
①?根据图中信息,最佳反应温度为__________________。
②?如何说明该反应中在实验选定的温度范围内,随反应温度的升高,产品活性氧含量先增加而随后减少_________________?。
参考答案:(1)富集空气中的CO2
(2)①C;b;②温度;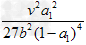 ;减小
;减小
(3)①30℃;②这是由于温度升高有利于尿素溶解及合成反应的进行,进而提高产品收率;但温度太高会导致过氧化氢分解,同时由于该反应为放热反应,升高温度会使平衡向逆反应方向移动,影响产品活性氧含量
本题解析:
本题难度:一般
5、选择题 一定条件下,可逆反应N2+3H2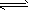 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
[? ]
A.加催化剂,V正、V逆都发生变化,且变化的倍数相等
B.加压,V正、V逆都增大,且V正增大的倍数大于V逆增大的倍数
C.降温,V正、V逆都减小,且V正减小的倍数大于V逆减小的倍数
D.增大氮气的浓度,V正、V逆都增大,且V正增大倍数大于V逆增大倍数;N2 转化率减小,H2转化率增大
参考答案:C
本题解析:
本题难度:一般