1、选择题 短周期元素aA2+、bB+、cC3-、dD-都具有相同电子层结构,则下列叙述正确的是
A.原子半径A>B>D>C
B.原子序数D>C>B>A
C.离子半径C>D>B>A
D.单质还原性A>B>D>C
参考答案:C
本题解析:试题分析:A选项,aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数A>B>D>C,A、B处于同一周期,C、D处于同一周期,且A、B处于C、D所在周期的相邻下一周期,同周期,原子序数越大原子半径越小,所以原子半径B>A,C>D,电子层越大原子半径越大,所以原子半径B>A>C>D,故A错误;B选项,aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则离子核外电子数相同,即a-2=b-1=c+3=d-1,原子序数A>B>D>C,故B错误;C选项,电子层结构相同,核电荷数越大,离子半径越小,核电荷数A>B>D>C,所以离子半径C3->D->B+>A2+,故C正确;D选项,A、B处于同一周期,A、B形成阳离子,则A、B为金属,原子序数A>B,单质还原性B>A,C、D处于同一周期,C、D形成阴离子,则C、D为非金属,原子序数D>C,单质氧化性D>C,故D错误。
考点:原子结构与元素周期率的关系
本题难度:困难
2、选择题 下列说法正确的是
A.用乙醇或CCl4可提取碘水中的碘单质
B.NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同
C.24Mg32S晶体中电子总数与中子总数之比为1∶1
D.H2S和SiF4分子中各原子最外层都满足8电子结构
参考答案:C
本题解析:乙醇和水互溶,不能作为萃取碘水中的萃取剂,A不正确。B不正确。氯化钠是离子晶体,破坏的是离子键。碳化硅是原子晶体,破坏的是极性键。D不正确,硫化氢中的氢元素是2电子稳定结构,所以正确的答案选C。
本题难度:一般
3、选择题 A、B、C、D、E是核电荷数依次增大的短周期元素,原子半径按D、E、B、C、A的顺序减小,B和E同主族,下列推断不正确的是
A.A、B、E一定在不同周期
B.D为第二周期
C.A、D可能在同一主族
D.C和D的单质可能化合为离子化合物
参考答案:B
本题解析:综合题目所给信息,五种元素在周期表中的相对位置可能为:
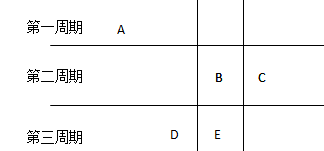
答案为B
本题难度:简单
4、选择题 下列化学式能真实表示物质分子组成的是?
①NaOH?②SiO2 ?③SO3?④He?⑤P? ⑥Na2O2
A.②③⑤
B.③⑤
C.③④
D.③④⑤
参考答案:C
本题解析:在离子晶体和原子晶体中不存在分子,所以其化学式不能代表物质的分子组成。只有在分子晶体中才存在分子,其化学式代表物质的分子组成。因为磷有多种同素异形体,所以⑤也不能代表物质的分子组成。答案是C。
本题难度:简单
5、选择题 仅用一种试剂即可将酒精、苯酚溶液、己烯、甲苯四种无色液体区别开,这种试剂是
A.FeCl3溶液
B.溴水
C.酸性KMnO4溶液
D.金属钠
参考答案:B
本题解析:
本题难度:简单