1、选择题 下列离子方程式书写正确的是
[? ]
A.向50 mL 1 mol・L-1 明矾溶液中滴入数滴0.1 mol・L-1 Ba(OH)2溶液
Al3++2SO42-+2Ba2++3OH- = Al(OH)3↓+2BaSO4↓
B.向KI与稀硫酸的混合溶液中通入氧气:4H++O2+6I-= 3I2+2H2O
C.a mol FeBr2溶液中通入a mol Cl2:2Fe2++2Br-+2Cl2 = Br2+2Fe3++4Cl-
D.在澄清石灰水中加入适量碳酸氢镁溶液:Ca2++ OH-+ HCO3- = CaCO3↓+H2O
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列离子方程式中正确的是
[?]
A.H2SO4与Ba(OH)2溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O
B.Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.向Na2CO3溶液中通入少量CO2:CO32-+CO2+H2O=2HCO3-
D.CH3COOH溶液与NaOH溶液反应:H++OH-=H2O
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列离子方程式书写正确的是
A.铁溶于盐酸中 2Fe + 6H+ = 2Fe3+ + 3H2↑
B.碳酸钠与硫酸溶液反应 CO32ˉ + H+ = CO2↑+ H2O
C.二氧化硫被烧碱溶液吸收 SO2 +2OHˉ= SO32ˉ + H2O
D.铜与稀硝酸反应 Cu + 8H+ + 2NO3ˉ= Cu2+ + 2NO↑ + 4H2O
参考答案:C
本题解析:A、违反客观事实,应为Fe2+,故错;B、电荷、质量都不守恒,故错;D、电荷不守恒,故错。故选C。
本题难度:一般
4、选择题 下列离子方程式中,只能表示一个化学反应的是
[? ]
①CO32-+2H+===CO2↑+H2O ②Ba2++2OH-+2H++SO42-===BaSO4↓+2H2O
③Ag++Cl-===AgCl↓ ④Fe+Cu2+===Fe2++Cu ⑤Cl2+H2O===H++Cl-+HClO
A、①③
B、②④
C、②⑤
D、⑤
参考答案:D
本题解析:
本题难度:简单
5、填空题 锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造图如图(a)所示。

回答下列问题:
(1)普通锌锰电池放电时发生的主要反应为:
Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是________,电解质的主要成分是______,正极发生的主要反应是________。
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是_______。
(2)图(b)表示回收利用废旧普通锌锰电池的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。
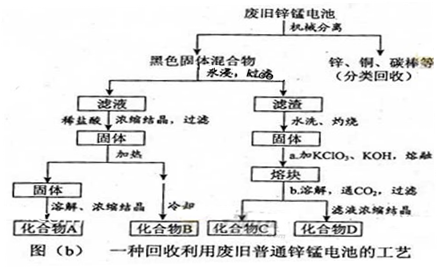
①图(b)中产物的化学式分别为A_______,B________。
②操作a中得到熔块的主要成分是K2MnO4。操作b中,绿色的K2MnO4溶液反应后生成紫色溶液和一种黑褐色固体,该反应的离子方程式为_______。
③采用惰性电极电解K2MnO4溶液也能得到化合物D,则阴极处得到的主要物质是?。(填化学式)
参考答案:(1)①Zn? NH4Cl? MnO2+NH4++e-=MnOOH+NH3
②碱性电池不易发生电解质的泄露,因为消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因为金属材料在碱性电解质中比在酸性电解质中的稳定性提高。
(2)①ZnCl2;NH4Cl②3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-③H2
本题解析:(1)根据化学方程式Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH,锌是负极材料,氯化铵是电解质的主要成分,二氧化锰和铵根离子在正极发生反应,MnO2+NH4++e-="MnOOH+" NH3。与普通锌锰电池相比,碱性锌锰电池的优点及其理由是碱性电池不易发生电解质的泄露,因为消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因为金属材料在碱性电解质中比在酸性电解质中的稳定性提高。
(2)废电池经机械分离后,加水溶解后再加稀盐酸,浓缩结晶得到氯化铵和氯化锌。氯化铵不稳定,受热易分解,所以B为氯化铵,A为氯化锌。绿色的K2MnO4溶液发生反应后生成紫色的高锰酸钾溶液和黑褐色的二氧化锰,该反应的离子方程式为3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-。采用惰性电极电解K2MnO4溶液,阴极氢离子得电子生成氢气。
本题难度:一般