1、选择题 下列关于氯水的说法正确的是
A.新制的氯水只含有氯气分子和水分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.光照氯水有气泡逸出,该气体主要是氯气
D.新制氯水久置后漂白性增强
参考答案:B
本题解析:略
本题难度:简单
2、实验题 某校化学兴趣小组为制备氯气设计了下列装置,
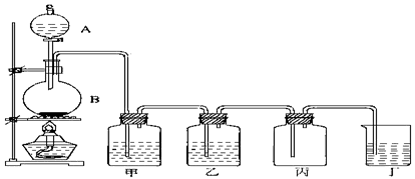
请回答问题:
(1)连接好装置,装药品之前,必须进行的一项操作步骤是____________________。
(2)A (仪器名称)是:__________________圆底烧瓶内发生反应的化学方程式为_____________________________________;
(3)_______(填甲或乙)中饱和食盐水的作用是_________________________________;
(4)尾气处理装置:用______________吸收多余的Cl2,防止污染空气。
参考答案:(1)检查装置的气密性
(2)分液漏斗,MnO2 + 4HCl(浓)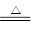 ?MnCl2 + Cl2↑+ 2H2O
?MnCl2 + Cl2↑+ 2H2O
(3)甲,除去Cl2中的HCl气体
(4)NaOH
本题解析:(1)化学实验装置连接后以后,在装药品之前,必须进行的一项操作步骤是检查装置的气密性,以防止漏气。
(2)根据A仪器的构造特点可知,A是分液漏斗。该装置是用来制备氯气的,所以圆底烧瓶内发生反应的化学方程式为MnO2 + 4HCl(浓)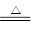 ?MnCl2 + Cl2↑+ 2H2O。
?MnCl2 + Cl2↑+ 2H2O。
(3)由于浓盐酸易挥发,生成的氯气中混有氯化氢气体,所以必须除去氯化氢。所以在甲装置中盛有饱和食盐水,用来除去Cl2中的HCl气体。
(4)氯气有毒,不能随意排放,以防止空气污染。所以必须用氢氧化钠溶液来吸收多余的Cl2,防止污染空气。
点评:该题是高考中的常见题型,难度不大。主要是考查学生对常见仪器以及实验室制备氯气的熟悉了解程度,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生规范严谨的实验设计能力和动手操作能力,提升学生的学科素养。
本题难度:一般
3、选择题 将少量氯水加入KI溶液中振荡,再加入CCl4,振荡,静置后观察到的现象是(?)
A.形成均匀的紫红色溶液
B.有紫色沉淀析出
C.液体分层,上层呈紫红色
D.液体分层,下层呈紫红色
参考答案:D
本题解析:氯与KI发生置换反应,生成碘单质和KCl,KCl溶解于水呈无色,碘被CCl4从水中萃取出来,是碘溶解在了CCl4中,而碘的CCl4溶液是紫色,CCl4的密度又大于水,所以会分层且下层是紫色。
点评:萃取的一般流程是:检漏,装萃取剂和被萃取的物质,振荡,静置分层,内外空气相通,分液。
本题难度:一般
4、选择题 下列物质不能使湿润的红色布条褪色的是( )
A.Cl2
B.氯水
C.Ca(ClO)2溶液
D.CaCl2溶液
参考答案:氯气可与水反应生成HClO,氯水中含有HClO,Ca(ClO)2溶液可与二氧化碳反应生成HClO,三者都可使品红褪色,而氯化钙溶液不具有漂白性,
故选D.
本题解析:
本题难度:一般
5、实验题 某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验。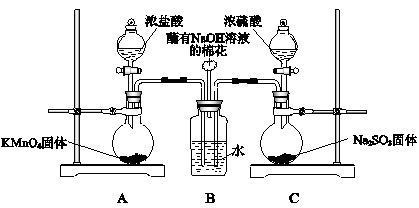
(1)装置A中的反应为2KMnO4+16HCl(浓) ="=" 2KCl+2MnCl2+5Cl2↑+8H2O,反应中的氧化剂是?,生成71 g Cl2转移的电子是?mol。
装置C中生成SO2,反应的化学方程式是?。
(2)装置B中蘸有NaOH溶液的棉花的作用是?。
(3)打开A、C中分液漏斗的活塞,一段时间后关闭活塞。待反应完全后,小组同学又继续如下实验。
①甲同学取适量B中溶液于试管中,向其中滴加少量AgNO3溶液,有白色沉淀生成。甲同学由此认为SO2和Cl2发生了反应,理由是该反应中生成了?(填离子符号)。
②乙同学认为甲同学的结论不合理,认为A中生成的Cl2中混有杂质,应该在装置A、B间增加一个然后再按甲同学的方法即可得到正确结论。
乙同学认为Cl2中混有的杂质是?,洗气瓶中盛有试剂的名称是?。
③ 丙同学则认为甲、乙两位同学的结论均不合理。丙同学取适量B中溶液于试管中,向其中滴加少量溶液X,有白色沉淀生成,则可得出结论,即SO2与Cl2同时通入水中,可以发生反应。溶液X是?(填选项序号)。
A.BaCl2溶液 ?B.Ba (OH)2溶液?C.Ba (NO3)2溶液?D.品红溶液
SO2与Cl2同时通入水中反应的化学方程式是?。
参考答案:(1)KMnO4?2? Na2SO3+H2SO4== Na2SO4+ SO2↑+ H2O
(2)尾气处理,防止污染空气 (3)①Cl―?②HCl?饱和食盐水?③A B? SO2+ Cl2+ 2H2O == 2HCl+H2SO4
本题解析:(1)在该反应中HCl中的Cl化合价为-1价,反应后一部分变为Cl2中的0价,化合价升高,失去电子,作还原剂,被氧化,另一部分化合价没有变化,只提供酸根离子,用来结合成盐。KMnO4?中的Mn化合价为+7价,反应后变为MnCl2的+2价,化合价降低,得到电子,作氧化剂,被还原。每产生5molCl2,转移电子10mol。生成71 g Cl2即1mol,转移的电子是2mol。装置C是制取SO2的装置,反应的化学方程式是Na2SO3+H2SO4== Na2SO4+ SO2↑+ H2O。(2)Cl2、SO2都是有毒的气体,都会造成大气污染。由于都会与NaOH发生反应,所以装置B中蘸有NaOH溶液的棉花的作用是尾气处理,防止污染空气。(3)①SO2和Cl2在装置B中发生反应SO2+ Cl2+ 2H2O == 2HCl+H2SO4,当加入AgNO3溶液时发生:HCl+ AgNO3="AgCl↓+" HNO3.溶液中含有Cl-离子。②浓盐酸有挥发性,所以乙同学认为Cl2中混有的杂质是HCl气体。除去Cl2中混有的杂质是HCl气体的方法是在洗气瓶中盛有试剂饱和食盐水。③BaCl2+ H2SO4=BaSO4↓+2HCl;? Ba (OH)2+ H2SO4=BaSO4↓+ 2H2O?溶液X是AB 。SO2与Cl2同时通入水中反应的化学方程式是SO2+ Cl2+ 2H2O == 2HCl+H2SO4。2与Cl2的实验室制法、化学性质、成分检验及尾气处理等知识。
本题难度:一般