1、选择题 m g二氧化锰与一定体积的浓盐酸反应,得到nL氯气(标准状况),可确定该反应中被还原的MnO2的物质的量是? (? )
A.m/55 mol
B.m/87 mol
C.n/11.2 mol
D.n/22.4 mol
参考答案:D
本题解析:MnO2+4HCl=MnCl2+Cl2+2H2O,得到nL氯气(标准状况),氯气的物质的量为n/22.4 mol,被还原的MnO2的物质的量和生成的氯气的物质的量相等,故选D。
本题难度:一般
2、选择题 向含有NaBr、KI的溶液中通入过量的Cl2,然后将溶液蒸干,并灼烧固体,最后得到的物质是
A.KCl
B.NaCl和KCl
C.NaCl和KBr
D.NaCl、KCl和I2
参考答案:B
本题解析:2NaBr+Cl2=2NaCl+Br2,Br2挥发后留下NaCl,2KI+Cl=1KCl+I2,灼烧固体后,碘升华,留下KCl,选B。
本题难度:一般
3、实验题 饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一。2005年的《化学教育》报道了如下实验研究:
一、定性研究:
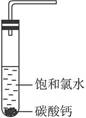
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请完成下列问题:
(1)反应后所得的溶液漂白性增强的原因是____________________________________。
(2)依据上述实验可推知,②的滤液中的溶质除CaCl2、HCIO外,还含有_________。
二、定量研究:
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150 mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加。
请完成下列问题:
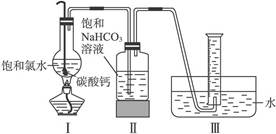
(3)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是____________________________________________________。
(4)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少A g,总共收集到标准状况下的CO2气体B L,发现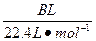 明显小于
明显小于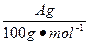 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________________________________________。
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________________________________________。
(5)实验后发现,装置Ⅱ中的液体增多了,其原因是____________________________________。
参考答案:(1)CaCO3消耗了氯水中的HCl,使Cl2+H2O HCl+HClO平衡向右移动,HClO浓度增大
HCl+HClO平衡向右移动,HClO浓度增大
(2)Ca(HCO3)2
(3)在导管末端再连接长导管,使导管的出口接近量筒底部
(4)碳酸钙与CO2反应生成的Ca(HCO3)2使生成CO2的物质的量小于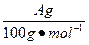
(5)从圆底烧瓶蒸出的水蒸气在广口瓶中冷凝、聚集
本题解析:本题是探索性的实验,研究定性和定量的问题和平衡移动的知识及观察能力、误差分析能力。
由于CaCO3消耗了氯水中的HCl,使Cl2+H2O HCl+HClO平衡向右移动,HClO浓度增大。过量的碳酸钙与释放出的CO2在水中反应生成Ca(HCO3)2。发现
HCl+HClO平衡向右移动,HClO浓度增大。过量的碳酸钙与释放出的CO2在水中反应生成Ca(HCO3)2。发现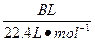 明显小于
明显小于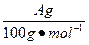 ,原因是CO2并没有完全释放出去。由Ⅰ到Ⅱ会有水蒸发出去,那么在Ⅱ中冷却,所以Ⅱ中的液体增多了。
,原因是CO2并没有完全释放出去。由Ⅰ到Ⅱ会有水蒸发出去,那么在Ⅱ中冷却,所以Ⅱ中的液体增多了。
本题难度:简单
4、选择题 下列对卤化氢的叙述不正确的是(?)
A.它们都是无色气体,在潮湿的空气中都可形成白雾
B.它们都易溶于水,其水溶液都是挥发性强酸
C.随着卤素原子核电荷数的增加,其热稳定性依次减弱
D.在标准状况下,等质量的气体,HF气体所占的体积最大
参考答案:B
本题解析:氢氟酸为弱酸,等质量时HF物质的量最大,故其体积最大。
本题难度:简单
5、选择题 将氯气制成漂白粉的主要目的是
[? ]
①使它转变成易溶于水的物质
②使它转变成稳定、便于储存的物质
③提高氯的质量分数
④提高漂白能力
A.①②
B.②③④
C.②③
D.②
参考答案:D
本题解析:
本题难度:简单