1、填空题 (10分)已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出B、D元素的名称:B?,D?。
(2)画出C元素的离子结构示意图?。
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式
?
(4)A、B、C三种元素形成的化合物所含的化学键类型为?。
(5)B、C、D三种元素的离子半径由大到小的排列顺序为?(用离子符号表示)。
参考答案:(1)B:氧、 D:铝(各1分)? (2) 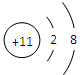 ?(2分)
?(2分)
(3)2A1 +? 2OH-+ 2H2O = 2AlO2- + 3H2↑(2分)
(4)离子键、共价键(各1分)? (5)O2->Na+?> Al3+?(2分)
本题解析:考查元素周期表的结构、原子核外电子的排布规律及元素周期律的应用。A元素原子形成的离子核外电子数为零,所以A是氢元素。E的单质为黄色晶体,易溶于二硫化碳,则E是单质硫。B与E同主族,所以B是氧元素。C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应,因此一定有铝元素。A与C同主族,且C的原子序数等于氧元素的,所以C是钠元素,则D是铝元素。核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,所以B、C、D三种元素的离子半径由大到小的排列顺序为O2->Na+?> Al3+。
本题难度:一般
2、选择题 元素X的一种核素的质量数为A,中子数为N,下列推断中不正确的是
A.这种核素的符号可表示为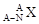
B.A可以表示这种核素的近似相对原子质量
C.A2+离子所含的电子数为A-N-2
D.A可表示X元素的近似相对原子质量
参考答案:D
本题解析:A正确,X的左上角为质量数,左下角为质子数,质量数=质子数+中子数;
B正确,质量数(A)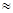 相对原子质量;C正确,A2+离子为阳离子,是A原子失去2个电子后形成的阳离子,其电子数为A-N-2;D错,A只能是质量数,不能表示元素的近似相对原子质量,元素的近似相对原子质量是指:元素的近似相对原子质量是按该元素的各种天然同位素的质量数和所占的原子的摩尔分数计算出来的平均值。
相对原子质量;C正确,A2+离子为阳离子,是A原子失去2个电子后形成的阳离子,其电子数为A-N-2;D错,A只能是质量数,不能表示元素的近似相对原子质量,元素的近似相对原子质量是指:元素的近似相对原子质量是按该元素的各种天然同位素的质量数和所占的原子的摩尔分数计算出来的平均值。
本题难度:一般
3、选择题 同温同压下,等质量的SO2与SO3相比较,下列叙述正确的是
A.含氧原子个数比为2∶3
B.含氧原子个数比为5∶6
C.含硫原子个数比为3∶4
D.含硫元素质量比为5∶4
参考答案:BD
本题解析:
设SO2与SO3质量各为1 g,SO2与SO3物质的量之比为n(SO2)∶n(SO3)=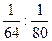 =5∶4,可知含硫元素质量比为5∶4;含氧原子个数比为
=5∶4,可知含硫元素质量比为5∶4;含氧原子个数比为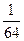 ×2∶(
×2∶(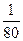 ×3)=5∶6。
×3)=5∶6。
本题难度:简单
4、选择题 下列原子中电离能最大的是( )
A.Be
B.C
C.Al
D.Si
参考答案:
B
本题解析:
判断元素原子的电离能大小,根据该元素所在周期表中的位置。同一周期从左到右,第一电离能逐渐增大;同一主族从上到下,电离能逐渐减小。
本题难度:一般
5、填空题 (8分)A元素原子M电子层上有3个电子,B元素与A元素的原子核外电子层数相同,B元素的原子最外层电子数为1。
(1)B元素的原子结构示意图为?;
(2)A元素在周期表中的位置?;
(3)含有B元素的化合物在无色火焰上灼烧时火焰呈?色。
(4)A和B的最高价氧化物的水化 物相互反应的离子方程式为:?。
物相互反应的离子方程式为:?。
参考答案:
(1)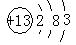
(2)第三周期ⅠA族
(3)黄
(4)Al(OH)3+OH-=AlO2-+3H2O
本题解析:略
本题难度:简单