?
�ο��𰸣���10�֣�
��1��Cl����2�֣�
��2��2Fe2+ + ClO��+ 2H+ �� 2Fe3+ + Cl��+ H2O ��2�֣�
SO42-��Cl-�����Һ�У�Ҫ����Cl-���ų�SO42-����
ʵ�鲽��
Ԥ������ͽ���
����1��ȡ������Ӧ�����Һ�������Թ�A�У��μӹ���Ba(NO3)2��Һ�������á���2�֣�
�а�ɫ�������ɣ����֣�
����2��ȡ�Թ�A���ϲ���Һ���Թ�B�У���ϡHNO3�ữ���Ӽ���AgNO3��Һ�������֣�
���а�ɫ�������ɣ���ͬѧ���Ʋ���ȷ����1�֣���
�����������1��NaClO����Ԫ��Ϊ+1�ۣ����Ļ�ԭ�������ȵĻ��ϼ�����νΪ0�۵������۵�Cl��.
(2)���⿼�������ӷ���ʽ����ƽ�����ӵļ��顣
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ����
[? ]
A��þ�뼫ϡ���ᷴӦ��������淋����ӷ���ʽΪ��4Mg+6H++NO3- =4Mg2++NH4++3H2O
B��25��ʱ����20 mL 0��1mol��L-1 H2SO4��Һ��30 mL 0��15mol��L-1 NaOH��Һ��ϣ�����Ϻ���Һ������䣬������Һ��pHΪ11
C����10 mL 0��1 mol��L-1 KAl(SO4)2��Һ��10 mL0��2 mol��L-1Ba(OH)2��Һ��ϣ��õ��ij�����Al(OH)3��BaSO4�����ʵ���֮��Ϊ1��2
D��Ũ�Ⱦ�Ϊ0��1 mol��L-1�Ĵ����CH3COONa��Һ�������ϣ���Һ�������й�ϵ��c��CH3COOH��+
2c��H+��=c��CH3COO-��+2c��OH-��
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ�����ӷ���ʽ��д��ȷ���ǣ�������
A������ͭ��Һ�мӹ����İ�ˮ��Cu2++2NH3?H2O�TCu��OH��2��+2NH4+
B����ʳ����������̼��ƵĴ��ڣ�CaCO3+2H+�TCa2++CO2��+H2O
C����������Һ��ͨ������������̼��C6H5O-+CO2+H2O�TC6H5OH+HCO3-
D���õ⻯�ص�����Һ��������������NO2-�Ĵ��ڣ�NO2-+2I-+2H+�TNO��+I2+H2O
�ο��𰸣�A������ͭ��Һ�мӹ����İ�ˮ�����ӷ�ӦΪCu2++4NH3?H2O�T[Cu��NH3��4]2++4H2O����A����
B����ʳ����������̼��ƵĴ��ڵ����ӷ�ӦΪCaCO3+2HAc�TCa2++CO2��+H2O+2Ac-����B����
C����������Һ��ͨ������������̼�����ӷ�ӦΪC6H5O-+CO2+H2O�TC6H5OH+HCO3-����C��ȷ��
D���õ⻯�ص�����Һ��������������NO2-�Ĵ��ڵ����ӷ�ӦΪ2NO2-+2I-+4H+�T2NO��+I2+2H2O����D����
��ѡC
���������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��д�ɻ�ѧ����ʽ��ȷ����
A��Cu2����2OH����Cu(OH)2? CuCO3��2NaOH Cu(OH)2?��Na2CO3 Cu(OH)2?��Na2CO3
B��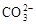 ��2H����CO2?��H2O BaCO3��2HCl ��2H����CO2?��H2O BaCO3��2HCl BaCl2��CO2?��H2O BaCl2��CO2?��H2O
C��Ca2����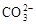 ��CaCO3?Ca(NO3)2��Na2CO3 ��CaCO3?Ca(NO3)2��Na2CO3 CaCO3?��NaNO3 CaCO3?��NaNO3
D��H����OH����H2O Ba(OH)2��H2SO4  BaSO4 ?��2H2O BaSO4 ?��2H2O
�ο��𰸣�C
���������̼��ͭ������ˮ��Ӧ���û�ѧʽ��ʾ��A����ȷ��̼�ᱵҲ������ˮ��Ӧ���û�ѧʽ��ʾ��B����ȷ�����ᱵ��������ˮ��ҲӦ���û�ѧʽ��ʾ��D����ȷ�����Դ�ѡC��
���������ж����ӷ���ʽ��ȷ���ķ���һ���ǣ���1����鷴Ӧ�ܷ�������2����鷴Ӧ��������Ƿ���ȷ����3���������ʲ���Ƿ���ȷ����4������Ƿ�����غ��ϵ���磺�����غ�͵���غ�ȣ�����5������Ƿ����ԭ��ѧ����ʽ��
�����Ѷȣ�һ��
5��ѡ���� ���з�Ӧ���ӷ���ʽ��ȷ����
A�����Ȼ�����Һ�м����������������Һ��Al3+ + 4OH�� ="=" AlO2�� + 2H2O
B��������Һ��ͨ�������̼��CO2 + H2O + 2C6H5O�� ��2C6H5OH + CO32��
C����С�մ���Һ�м��������Һ��HCO3�� + H+ ="=" CO2��+ H2O
D�����廯������Һ��ͨ�����������Fe2+ + 2Br�� + 2Cl2 ="=" Fe3+ + Br2 + 4Cl��
�ο��𰸣�A
������������ӵ�����ǿ��̼�����Ƶģ�����B�е���������̼�����ƣ�����ȷ��������������ʣ��û�ѧʽ��ʾ��C����ȷ��D�е�ɲ��غ㣬Ӧ����2Fe2+ + 4Br�� + 3Cl2��2Fe3+ +2Br2 + 6Cl������ѡA��
�����Ѷȣ�һ��
|