1、选择题 下列离子方程式中书写正确的是( )
A.实验室用碳酸钙和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O
B.铁和稀硫酸反应:Fe+2H+=Fe3++H2↑
C.过氧化钠与水的反应:2Na2O2+2H2O=4Na++4OH-+O2↑
D.向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓
参考答案:A.实验室用碳酸钙和稀盐酸制取CO2的离子反应为2H++CaCO3=CO2↑+H2O+Ca2+,故A错误;
B.铁和稀硫酸反应的离子反应为Fe+2H+=Fe2++H2↑,故B错误;
C.过氧化钠与水的反应的离子反应为2Na2O2+2H2O=4Na++4OH-+O2↑,故C正确;
D.向AlCl3溶液中加入过量的NaOH溶液的离子反应为Al3++4OH-=AlO2-+2H2O,故D错误;
故选C.
本题解析:
本题难度:一般
2、选择题 下列用来表示物质变化的化学反应中正确的是
A.表示中和热的热化学方程式:H++OH-=H2O △H=-57.3kJ・mol-1
B.硫酸氢铵溶液与少量氢氧化钠溶液混合共热的离子方程式:NH4++OH-=NH3↑+H2O
C.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+
D.足量酸性高锰酸钾溶液与双氧水反应的离子方程式:2MnO4-+5H218O2+6H+=2Mn2++518O2↑+8H2O
参考答案:D
本题解析:书写热化学方程式时,需标明物质的状态,A错;硫酸氢铵中的氢也会与NaOH反应,离子方程式未表示出来,B错;强碱性溶液中不可能生成H+,C错;根据氧化还原反应电子得失守恒,MnO4-恰好将H2O2中的O全部氧化为O2,D正确。
本题难度:一般
3、填空题 Ⅰ.铁盐、亚铁盐是实验室常用的药品。
请根据题意,完成下列填空:
(1)向酸化的FeCl3溶液中逐滴加入KI溶液,溶液变成棕褐色。该反应的离子方程式为________________。
(2)向酸化的FeSO4溶液中加几滴硫氰化钾溶液,没有什么明显变化,再滴加双氧水,溶液变血红色。继续滴加双氧水,血红色逐渐褪去,且有气泡产生。
写出上述变化中,有关反应的离子方程式:
①____________________________________;
②Fe3++3SCN-=Fe(SCN)3;
③11H2O2+2SCN-=2SO42―+2CO2↑+N2↑+10H2O+2H+
若生成1 mol N2,H2O2和SCN-的反应中转移电子的物质的量是________ mol。
(3)根据以上实验,推断Fe2+、I-和SCN-的还原性由强到弱的顺序为________。
Ⅱ.某课题组利用Fe粉和KNO3溶液反应,模拟地下水脱氮过程,探究脱氮原理。
(4)实验前:①先用0.1 mol・L-1 H2SO4洗涤Fe粉,其目的是__________,然后用蒸馏水洗涤至中性;②将KNO3溶液的pH调至2.5;③为防止空气中的O2对脱氮的影响,应向KNO3溶液通入________(写化学式)。
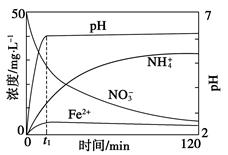
(5)如图表示足量Fe粉还原上述KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前该反应生成的阳离子分别是________、________。t1时刻后,该反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是__________________。
参考答案:Ⅰ.(1)2Fe3++2I-=2Fe2++I2
(2)2Fe2++H2O2+2H+=2Fe3++2H2O 22
(3)I->Fe2+>SCN-
Ⅱ.(4)除去Fe粉表面的铁锈(Fe2O3)等杂质 N2
(5)Fe2+、NH4+ 溶液的pH增大,Fe2+形成了Fe(OH)2(或与溶液中OH-结合)
本题解析:(1)Fe3+能氧化I-,离子方程式为2Fe3++2I-=2Fe2++I2。
(2)Fe2+和SCN-不反应,当加入H2O2时,发生2Fe2++2H++H2O2=2Fe3++2H2O,然后Fe3+和SCN-反应生成血红色溶液,继续滴加H2O2,SCN-被氧化。根据反应③,当有1 mol N2生成时,转移电子的物质的量为11×2×[-1-(-2)] mol=22 mol。(注:根据氧化剂计算方便)
(3)根据(1)(2)中方程式可得还原性I->Fe2+>SCN-。(根据还原剂还原性大于还原产物还原性)
(4)因为Fe粉表面有铁锈,所以应预先用H2SO4除去。因为Fe粉在溶液中能被O2氧化,所以应通入N2排除O2的干扰。
(5)根据图中信息,Fe粉被NO3―氧化成Fe2+,其本身被还原成NH4+,在此过程中碱性增强,因为有OH-生成,Fe2+与之反应生成Fe(OH)2沉淀,造成Fe2+的浓度变化不大。
本题难度:困难
4、选择题 已知氧化性:Br2>Fe3+>I2,向含有a mol FeI2的溶液中加入含b mol Br2的溴水,下列判断或相应的离子方程式正确的是
A.当a=2,b=1时,离子方程式为:2Fe2++Br2→2Fe3++2Br-
B.如果反应后的溶液中存在c(Fe2+)=c(Fe3+),则4/5<a/b<1
C.当a=1,b=2时,离子方程式为:2Fe2++4I-+3Br2→2Fe3++2I2+6Br-
D.当a=2,2<b<3时,溶液中铁元素以两种离子形式存在,且一定是c(Fe3+)>c(Fe2+)
参考答案:C
本题解析:A选项,根据题意可知,还原性I->Fe2+>Br-,故离子反应方程式为2I-+Br2=2Br-+I2。B选项,若反应后的溶液中存在c(Fe2+)=c(Fe3+),则发生反应方程式为4FeI2+5Br2=4I2+10Br-+2Fe2++2Fe3+,故只有在a/b=4/5时满足,故错误。C选项,正确。D选项,当a=2,b=2时,溶液中全部为Fe2+。当a=2,b=3时,溶液中有1/2Fe2+,故当a=2,2<b<3时,溶液中铁元素以两种离子形式存在且一定是c(Fe3+)<c(Fe2+)。
本题难度:一般
5、选择题 用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式2H++SO32-=H2O+SO2↑的反应个数有
A.4个
B.5个
C.8个
D.12个
参考答案:C
本题解析:化学方程式仅表示一定物质间的某个反应,而两离子方程式表示了所所有同一类的反应。用上述物质发生的化学反应有(1)硝酸+亚硫酸钠=硝酸钠+水+二氧化硫;(2)硝酸+亚硫酸钾=硝酸钾+水+二氧化硫;(3)硫酸+亚硫酸钠=硫酸钠+水+二氧化硫;(4)硫酸+亚硫酸钾=硫酸钾+水+二氧化硫;(5)盐酸+亚硫酸钾=氯化钾+水+二氧化硫;(6)盐酸+亚硫酸钠=氯化钠+水+二氧化硫;(7)硫酸氢钠+亚硫酸钠=硫酸钠+水+二氧化硫;(8)硫酸氢钾+亚硫酸钾=硫酸钾+水+二氧化硫;因为亚硫酸钡难容,不能写成SO32-形式,所以无钡盐。正确选项为:C。
本题难度:一般