1������� A��B��C��DΪ�������ڳ�ϡ���������Ԫ�أ����ǵ�ԭ������������������Ԫ����ֻ��CΪ����Ԫ�أ�A��C��������������ȣ�B��D����ͬ���壻C��D��Ԫ��ԭ�ӵ�������֮��ΪA��B��Ԫ��ԭ�ӵ�������֮�͵�3������ش��������⣺
��1��A��Ԫ�ط���Ϊ______��B��ԭ�ӽṹʾ��ͼ______��
��2��C2B2�к��еĻ�ѧ����______��д��C2B2��A2B��Ӧ�����ӷ���ʽ______��
��3��A��B��C��D���Ӱ뾶�ɴ�С��˳��Ϊ�������ӷ��ű�ʾ��______��
��4���û�ѧ����ʽ֤��Ԫ��ԭ�ӵĵõ�������Bǿ��D______��
�ο��𰸣�A��B��C��DΪ�������ڳ�ϡ���������Ԫ�أ����ǵ�ԭ��������������CΪ����Ԫ�أ�A��C��������������ȣ�λ��ͬ���壬��CΪNa��AΪH��B��D����ͬ���壬��B��������Ϊx����D��������Ϊx+8��C��D��Ԫ��ԭ�ӵ�������֮��ΪA��B��Ԫ��ԭ�ӵ�������֮�͵�3��������11+x+8=��1+x����3�����x=8����BΪO��DΪS��
��1��AΪH��BΪO����ԭ�ӽṹʾ��ͼΪ
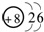
���ʴ�Ϊ��H��
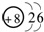
��
��2��C2B2ΪNa2O2������������������������Ӽ���ϣ�O��O֮���Թ��ۼ���ϣ���ˮ��Ӧ�����ӷ�ӦΪ2Na2O2+2H2O�T4Na++4OH-+O2����
�ʴ�Ϊ�����Ӽ������ۼ���2Na2O2+2H2O�T4Na++4OH-+O2����
��3�����Ӳ�Խ�࣬���Ӱ뾶Խ������ͬ�����Ų������ӣ�ԭ������������Ӱ뾶С��
�����Ӱ뾶ΪS2-��O2-��Na+��H+��
�ʴ�Ϊ��S2-��O2-��Na+��H+��
��4������Ԫ�ص��ʵ��û���Ӧ��˵���õ���������ǿ������H2S+O2�TH2O+S�����ʴ�Ϊ��H2S+O2�TH2O+S����
���������
�����Ѷȣ�һ��
2��ѡ���� ����Ԫ��R��ԭ�������ʽ������ʽ��ʾ��
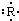
����Ԫ����ɵ��������ʣ������ʽ�϶�������ǣ�������
A�����������ʽ����ΪH3RO4
B�����������ʽ����ΪHRO3
C����̬�⻯�����ʽΪRH5
D��������������ʽΪR2O5
�ο��𰸣�Ԫ��R��ԭ�������ʽ������ʽ��ʾ��
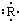
�����ݵ���ʽ��֪ԭ������������5��������ϼ�ӦΪ+5�ۣ���ͻ��ϼ�Ϊ-3�ۣ���
A������ϼ�Ϊ+5�ۣ���ΪPԪ�أ����������ʽΪH3RO4����A��ȷ��
B������ϼ�Ϊ+5�ۣ���ΪNԪ�أ����������ʽΪHRO3����B��ȷ��
C����ͻ��ϼ�Ϊ-3�ۣ�����̬�⻯�����ʽΪRH3����C����
D������ϼ�Ϊ+5�ۣ���������������ʽΪR2O5����D��ȷ��
��ѡC��
���������
�����Ѷȣ���
3��ѡ���� ��֪X+��Y2+��Z-��W2-�������Ӿ�������ͬ�ĵ��Ӳ�ṹ�����й���X��Y��Z��W����Ԫ�ص�����������ȷ���ǣ�������
A��ԭ�Ӱ뾶��X��Y��Z��W
B��ԭ��������Y��X��Z��W
C��ԭ��������������Z��W��Y��X
D�������ԣ�X��Y
�ο��𰸣�X+��Y2+��Z-��W2-�������Ӿ�������ͬ�ĵ��Ӳ�ṹ����X��Y����һ���ڣ�Y��ԭ����������X��ԭ��������Z��W����һ���ڣ�Z��ԭ����������W��ԭ��������
A�����Ӳ�Խ�࣬�뾶Խ��ͬ���ڴ�������ԭ�Ӱ뾶�ڼ�С����ԭ�Ӱ뾶ΪX��Y��W��Z����A����
B����λ�ÿ�֪��ԭ������ΪY��X��Z��W����B��ȷ��
C��X+��Y2+��Z-��W2-�������Ӷ�Ӧ��������۷ֱ�Ϊ+1��+2��+7��+6��������۵�����������������ԭ������������ΪZ��W��Y��X����C��ȷ��
D��ͬ���ڴ������ҽ������ڼ�С���������ΪX��Y����D��ȷ��
��ѡA��
���������
�����Ѷȣ�һ��
4������� A��B��C��D��E��F���ֶ���������Ԫ�ص�ԭ����������������֪��
��A��B���γɶ�����̬�����B��D���γ����ֳ�����̬�����D��E���γ��������ӻ����
��B��C��D��ͬһ�������ڵ�����Ԫ�أ�����C��E��ԭ������֮�͵���A��F��ԭ������֮�ͣ�
��EԪ�ص�ԭ�Ӱ뾶����FԪ�ص�ԭ�Ӱ뾶��
��ش�
��1��EԪ����Ԫ�����ڱ���λ����______��E��D��ԭ�Ӹ���Ϊ1��1�γɵĻ�����ĵ���ʽ��______�������Ļ�ѧ����______��
��2��B��D�γɵ�������̬�������к�������ԭ�ӵĻ�����Ľṹʽ��______������ͨ������NaAlO2��Һ��������______�����ӷ���ʽΪ______��
��3����A��C��F����Ԫ�������һ�����ӻ���������������ӵķ����ǣ������ӷ���ʽ��ʾ��______��
��4��������ͬ��ԭ��������ͬ�ĵ������IJ�ͬ���ӳ�Ϊ�ȵ����壮д������������Ԫ���γɵ���������CԪ�صĵ��ʻ�Ϊ�ȵ������һ�����ӵĻ�ѧʽ��______��
�ο��𰸣�A��B��C��D��E��F���ֶ���������Ԫ�ص�ԭ��������������A��B���γɶ�����̬�������AΪH��BΪC��B��D���γ����ֳ�����̬�������DΪO��D��E���γ��������ӻ��������EΪNa��B��C��D��ͬһ�������ڵ�����Ԫ�أ���CΪN��C��E��ԭ������֮�͵���A��F��ԭ������֮�ͣ�����F��ԭ������Ϊ7+11-1=17������FΪCl��
��1��Naλ��Ԫ�����ڱ��е������ڵڢ�A�壬��O��ԭ�Ӹ���Ϊ1��1�γɵĻ�����ΪNa2O2�������ʽΪ
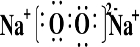
���������Ӽ����ۼ���
�ʴ�Ϊ���������ڵڢ�A�壻
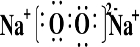
�����Ӽ����ۼ���
��2��B��D�γɵ�������̬�������к�������ԭ�ӵĻ�����ΪCO2����ṹʽΪO=C=O������ͨ������NaAlO2��Һ��Ӧ��������������������۲쵽��ɫ���������ӷ�Ӧ����ʽΪ
CO2+2AlO2-+3H2O�T2Al��OH��3��+CO32-���ʴ�Ϊ��O=C=O����ɫ�������ɣ�CO2+2AlO2-+3H2O�T2Al��OH��3��+CO32-��
��3��A��C��F����Ԫ�������һ�����ӻ�����ΪNH4F��һ��������Ӧ���ɰ��������飬���ӷ�ӦΪNH4++OH-?��?.?NH3��+H2O��
�ʴ�Ϊ��NH4++OH-?��?.?NH3��+H2O��
��2��������ͬ��ԭ��������ͬ�ĵ������IJ�ͬ���ӳ�Ϊ�ȵ����壬N2��ԭ����Ϊ2��������Ϊ7��2=14����CO��ԭ����Ϊ2��������Ϊ6+8=14������Ϊ�ȵ����壬�ʴ�Ϊ��CO��
���������
�����Ѷȣ�һ��
5��ѡ���� ��������Ϊ����Ԫ�صĺ˵����������ԭ�Ӻ�������������������
[? ]
A��8
B��14
C��20
D��34
�ο��𰸣�AD
���������
�����Ѷȣ���