1、选择题 核外电子是有规律地进行排布的,它们分层排布在K、L、M、N、O…层上,下列叙述正确的是( )
A.K层上容纳的电子数只能是2个
B.K层上容纳的电子数可以超过2个
C.L层上最多只能容纳8个电子
D.最外层上容纳的电子数可以超过8个
参考答案:C
本题解析:
本题难度:简单
2、选择题 化学用语是学习化学的重要工具。以下化学用语表示错误的是
[? ]
A.质量数之和是质子数之和两倍的水分子符号可能是:D216O
B.NaHCO3水溶液呈碱性的原因:HCO3-+H2O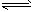 H3O++CO32-
H3O++CO32-
C.基态硫离子的电子排布式:1s22s22p63s23p6
D.熔融状态下硫酸氢钠的电离方程式:NaHSO4(熔融)=Na++HSO4-
参考答案:B
本题解析:
本题难度:简单
3、填空题 化学-物质结构
氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应.
请回答下列问题:
(1)写出铬原子的基态电子排布式______,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有______(填元素符号),其中一种金属的晶胞结构如图所示,该晶胞中含有金属原子的数目为______,配位数为______.
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是______(填“极性”或“非极性”)分子.
(3)在①苯?②CH3OH?③HCHO?④CS2⑤CCl4⑥CH3Cl?⑦HCOOH七种有机物质中,碳原子采取sp2杂化的分子有______(填序号),CS2分子的空间构型是______.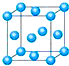
参考答案:(1)Cr的原子序数为24,根据能量最低原理可知基态原子的电子排布式为1s22s22p63s23p63d54s1,
铬原子的最外层电子数为1,位于第四周期,
与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有K、Cu,
晶胞中原子分布于顶点和面心,则原子的数目为:8×18+6×12=4,
与顶点金属原子距离最近的原子位于面心位置,则配位数为8×32=12,
故答案为:1s22s22p63s23p63d54s1;?K、Cu;4;12;
(2)CCl4、CS2等为非极性分子,CrO2Cl2能与CCl4、CS2等互溶,根据相似相溶可知,CrO2Cl2为非极性分子,
故答案为:非极性;
(3)①苯中C形成3个δ键,为sp2杂化,②CH3OH中C形成4个δ键,为sp3杂化,
③HCHO中C形成3个δ键,为sp2杂化,④CS2中C形成2个δ键,为sp杂化,
⑤CCl4中C形成4个δ键,为sp3杂化,⑥CH3Cl中C形成4个δ键,为sp3杂化
⑦HCOOH中C形成3个δ键,为sp2杂化,
所以碳原子采取sp2杂化的分子有①③⑦,
CS2分子中C形成2个δ键,孤电子对数为4-2×22=0,价层电子对为2,所以CS2分子为直线形.
故答案为:①③⑦;?直线形.
本题解析:
本题难度:一般
4、简答题 已知:A-F都是周期表中前四周期的元素,它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子具有相同的电子层结构.F3+离子的M层3d轨道电子为半充满状态.请根据以上信息,回答下列问题:(答题时,用所对应的元素符号表示)
(1)A、B、C的电负性由小到大的顺序为______.
(2)D元素的原子核外共有______种不同运动状态的电子、______种不同能级的电子.
(3)H2S和C元素的氢化物(分子式为H2C2)的主要物理性质比较如下:
| 熔点 | 沸点 | 标准状况时在水中的溶解度
H2S
187
202
2.6
H2C2
272
423
以任意比互溶
|
H2S和H2C2的相对分子质量基本相同,造成上述物理性质差异的主要原因是______.AC2中心原子的杂化方式为______,某离子与AC2互为等电子体,且能用于鉴别F3+,写出该离子的电子式______.
(4)写出E的电子排布式:______.
(5)F和X(质子数为25)两元素的部分电离能数据列于表:
| 元素 | X | F
|
电离能kJ?mol-1
I1
717
759
I2
1509
1561
I3
3248
2957
|
比较两元素的I2、I3可知,气态X2+再失去一个电子比气态F2+再失去一个电子难.对此,你的解释是______.
参考答案:A、B、C、D、E、F都是周期表中前四周期的元素,它们的原子序数依次增大.A、C原子的L层有2个未成对电子,为碳元素和氧元素,原子序数A<C,所以A为C元素,C为O元素;
B的原子序数介于A与C之间,所以B为N元素;
D的二价阳离子与C的阴离子具有相同的电子层结构,D为Mg元素,D与E同主族,原子序数D<E,则E为Ca元素;
F3+离子M层3d轨道电子为半满状态,则F为Fe元素;
即A为C元素,B为N元素,C为O元素,D为Mg元素,E为Ca元素,F为Fe元素;
(1)A为C元素,B为N元素,C为O元素,同一周期元素,元素的电负性随着原子序数的增大而增大,所以电负性大小顺序是C<N<O,
故答案为:C<N<O;
(2)D为Mg元素,原子中电子的运动状态种类与其电子数相等,所以镁原子核外有12种不同运动状态的电子,有1s、2s、2p、3s四种不同能级的电子,
故答案为:12;4;
(3)C为O元素,非金属性较强,对应的氢化物能形成氢键,且与水分子之间也可以形成氢键,所以H2O2的沸点比H2S高;
CO2中心原子价层电子对个数是2,所以中心原子的杂化方式为sp,某离子与CO2互为等电子体,且能用于鉴别Fe3+的离子为SCN-,该离子的电子式为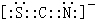 ,
,
故答案为:H2O2分子间存在氢键,与水分子可形成氢键;sp;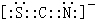 ;
;
(4)E为Ca元素,钙原子核外有20个电子,根据构造原理知,其核外电子排布式为1s22s22p63s23p64s2,
故答案为:1s22s22p63s23p64s2;
(5)质子数为25的元素为Mn,由于Mn2+的3d轨道电子排布为半满状态较稳定,难以失去电子,
故答案为:Mn2+的3d轨道电子排布为半满状态较稳定.
本题解析:
本题难度:一般
5、选择题 关于硫原子核外电子的叙述错误的是( )
A.排布在K、L、M三个电子层上
B.3p亚层上有2个空轨道
C.共有16种不同的运动状态
D.共有5种不同的能量
参考答案:B
本题解析:
本题难度:简单