1、填空题 (16分)Ⅰ.下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的某性质)
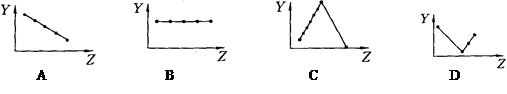 ?
?
把与下面元素有关性质相符的曲线标号填入相应括号中:
⑴ⅡA族元素的最外层电子数 (? )?⑵第三周期元素的最高化合价(?)
⑶第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径(?)
⑷第二、三周期元素随原子序数递增原子半径的变化(不包括惰性气体) (?)
⑸碱金属的阳离子氧化能力(不包括钫)(?)?
Ⅱ.下图是元素周期表的一部分
?
| ?
| ?
|
?
| 
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
⑴请在表中画出金属与非金属的交界线?⑵请在表中标出第VIII的位置?
⑶在表中标出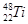 的位置
的位置
参考答案:Ⅰ.⑴(? B? ) (2分)?⑵( C )(2分)?⑶( E )(2分)?
⑷( G )(2分)?⑸( A )(2分)
Ⅱ. ⑴略(2分)⑵略(2分)?⑶略(2分)
本题解析:Ⅰ.⑴ⅡA族元素的最外层电子数都是2个,所以答案选B。
(2)第三周期元素的最高化合价,自左向右逐渐升高,但0族最低,所以答案选C。
(3)核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小。电子层数越多,离子半径越大,所以答案选E。
(4)同周期自左向右原子半径逐渐减小,所以答案选G。
(5)金属性越强,相应阳离子的氧化性越弱,同主族自上而下金属性逐渐增强,所以答案选A。
Ⅱ. (1)、(2)参照教材
(3)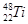 位于正确的第四周期第ⅣB。
位于正确的第四周期第ⅣB。
本题难度:一般
2、填空题 (11分)有四种短周期元素,它们的结构、性质等信息如下表所述:
元素
| 结构、性质等信息
|
A
| 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂
|
B
| B与A同周期,其最高价氧化物的水化物呈两性
|
C
| 元素的气态氢化物极易溶于水,可用作制冷剂
|
D
| 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂
|
请根据表中信息填写:
(1)A原子的核外电子排布式
____________________________________________________________。
(2)B元素在周期表中的位置__________;离子半径:B______A(填“大于”或“小于”)。
(3)C原子的电子排布图是__________?,其原子核外有______个未成对电子,能量最高的电子为______轨道上的电子,其轨道呈______?形。
(4)D原子的电子排布式为________,D-的结构示意图是______ 。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为______?_,与D的氢化物的水化物反应的化学方程式为_______________。
参考答案:(1)1s22s22p63s1 (2)第三周期第ⅢA族 小于
(3)  3 p 哑铃
3 p 哑铃
(4)1s22s22p63s23p5或[Ne]3s23p5 
(5)NaOH+Al(OH)3===NaAlO2+2H2O? 3HCl+Al(OH)3===AlCl3+3H2O
本题解析:根据题中信息可推出:A为Na,B为Al,C为N,D为Cl。
(1)A为Na,其核外电子排布式为1s22s22p63s1。
(2)B为Al,在元素周期表中的位置为第三周期第ⅢA族,Na+与Al3+核外电子排布相同,核电荷数Al3+大于Na+,故r(Al3+)<r(Na+)。
(3)C为N,其电子排布图为 ,其中有3个未成对电子,能量最高的为p轨道上的电子,其轨道呈哑铃形。
,其中有3个未成对电子,能量最高的为p轨道上的电子,其轨道呈哑铃形。
(4)D为Cl,其核外电子排布式为1s22s22p63s23p5,简化电子排布式为[Ne]3s23p5,Cl-的结构示意图为 .
.
(5)本题考查Al(OH)3与NaOH和HCl反应的方程式,
Al(OH)3+NaOH===NaAlO2+2H2O,Al(OH)3+3HCl===AlCl3+3H2O。
本题难度:一般
3、选择题 下列各组元素的原子随着原子序数的递增,有关递变不正确的是(?)
A.最高正价:P<S<Cl<Ar
B.原子半径:C>N>O>F
C.金属性:Na<K<Rb<Cs
D.最外层电子数:Na<Mg<Al<Si
参考答案:A
本题解析:A不正确,Ar是稀有气体,没有正价,其余选项都是正确的,答案选A。
点评:该题是中等难度的试题,主要是考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。有助于培养学生的逻辑思维能力和应试能力,提高学生的答题效率。
本题难度:一般
4、选择题 下列物质属于混合物的是
A.氯水
B.液氯
C.氧气
D.氯化氢
参考答案:A
本题解析:
本题难度:一般
5、选择题 两种短周期元素组成的化合物中,原子个数比为1:3,若两种元素的原子序数分别为a和b,则a和b的关系可能是? ①a=b+3;? ②a+b=8;? ③a+b="30" ;? ④a=b+8
A.②③
B.③④
C.②③④
D.①②③④
参考答案:C
本题解析:略
本题难度:一般