1、推断题 已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。
请回答下列问题:
(1)X元素原子基态时的电子排布式为____________,该元素的符号是________________;
(2)Y元素原子的价层电子的轨道表示式为_______________,该元素的名称是_____________;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为________________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是_________________________;
(5)比较X的氢化物与同族第二、三周期元素所形成的氢化物稳定性、沸点高低并说明理由________________________________。
参考答案:(1)1s22s22p63s23p63d104s24p3;As
(2)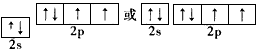 ;氧
;氧
(3)三角锥形
(4)As2O3+6Zn+6H2SO4==2AsH3↑+6ZnSO4+3H2O
(5)稳定性:NH3> PH3> AsH3,因为键长越短,键能越大,化合物越稳定沸点:NH3> AsH3> PH3,
NH3可以形成分子间氢键,沸点最高,AsH3相对分子质量比PH3大,分子间作用力大,因而AsH3的沸点比PH3高
本题解析:
本题难度:困难
2、填空题
族
周期 | IA | | 0
1
H
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
He
2
Li
Be
B
C
N
O
F
Ne
3
Na
Mg
Al
Si
P
S
Cl
Ar
|
上表为1~18号元素.有A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18;A原子核内仅有1个质子;B原子的最外层电子数为最内层电子数的2倍;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍;E元素的最外层电子数是其电子层数的三分之一.
(1)试推断它们各是什么元素,写出它们的元素符号:
A______、B______、C.______、D______、E______.
(2)写出A分别与B、C、D所形成化合物的化学式:______、______、______
(3)写出A、C、D形成的化合物与A、D、E形成的化合物间相互反应的化学方程式.______.
参考答案:1~18号元素中,有A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18,A原子核内仅有1个质子,A为H元素;B原子的最外层电子数为最内层电子数的2倍,B有2个电子层,最外层电子数为4,故B为C元素;D原子有两个电子层,最外层电子数是次外层电子数的3倍,最外层电子数为6,故D为O元素;E元素处于第三周期,E元素的最外层电子数是其电子层数的三分之一,故最外层电子数为2,故E为Mg元素;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,故C的最外层电子数为1+4=5,原子序数小于O元素,故C为N元素,则:
(1)由上述分子可知,A为H元素,B为C元素,C为N元素,D为O元素,E为Mg元素,
故答案为:H,C,N,O,Mg;
(2)H分别与C、N、O所形成化合物的化学式为CH4、NH3、H2O等,
故答案为:CH4、NH3、H2O;
(3)A、C、D形成的化合物与A、D、E形成的化合物间相互反应,故A、C、D形成的化合物为HNO3,A、D、E形成的化合物
为Mg(OH)2,二者发生反应的方程式为:Mg(OH)2+2HNO3=Mg(NO3)2+2H2O,
故答案为:Mg(OH)2+2HNO3=Mg(NO3)2+2H2O.
本题解析:
本题难度:一般
3、推断题 已知X、Y、Z、W、U五种元素均位于元素周期表的前四周期。X原子的最外层p能级上有3个未成对电子。Y与X处于同周期,Y原子获得2个电子可以形成与氖原子相同的电子层结构的离子。Z是地壳中含量最多的金属元素。W的单质是人类用于生产的第一种金属,它是1939年在河南安阳殷墟出土的鼎的主要成分。U元素的单质在现代电池制造工业上具有不可或缺的地位,该元素对人体的免疫功能有调节作用,能促进儿童的正常发育。请回答下列问题:
(1)X原子的第一电离能比Y原子的第一电离能_______ (填“高”、“低”或“相同”),原因是__________________ ,Y3分子的空间构型为_________________;
(2)通常不用含有W元素的金属或合金来做焰色反应,原因是______________,许多金属盐能用来做焰火 的原因是______________;
(3)Z与U的氢氧化物都属于两性氢氧化物,设计实验鉴别ZCl3溶液与UCl2溶液_____________;
(4)工业上通常采用熔融状态的Z的氧化物而不是氯化物制取Z的原因是__________________;
(5)Y的简单氢化物在固态时的密度比液态时的密度__________(填“大”、“小”或“相同”),原因是____________________。
参考答案:(1)高;氮原子核外电子排布处于半充满状态,原子所具有的能量较低;折线形
(2)Cu元素及其化合物本身具有颜色反应;电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长(可见光区域)的光的形式释放能量
(3)分别取少量试样于小试管中,加入过量的氨水,有白色胶状沉淀生成的是AlCl3溶液,先有白色沉淀生成继而沉淀溶解的是ZnCl2溶液
(4)AlCl3属于分子晶体(或极性分子),在熔融状态时不能导电,Al2O3属于离子化合物,在熔融状态下能导电
(5)小;在液态水中,经常是几个水分子通过氢键结合起来,形成(H2O)n,在固态水(冰)中,水分子大范围地以氢键互相联结,形成相当疏松的晶体,从而在结构中有许多空隙,造成体积膨胀、密度减小
本题解析:
本题难度:一般
4、选择题 超重元素“稳定岛”的假设预言:自然界中可能存在着原子序数为114的元素的稳定同位素208X.1999年人们发现了114号元素,有力地支持了“稳定岛”学说.请你根据已知的元素周期律预测208X在元素周期表中的位置
A.第八周期Ⅷ族
B.第七周期ⅥA族
C.第七周期ⅣA族
D.第六周期ⅠB族
参考答案:C
本题解析:根据已有的元素周期律,第七周期如果排满,应排到118号,即118号元素应位于第七周期0族(第18列),由此可知114号元素应位于同一周期,第ⅣA族(第14列).
本题难度:一般
5、选择题 甲乙两种非金属:①甲比乙容易与H2化合;②甲的氢化物比乙的氢化物稳定③甲的最高价氧化物对应的水化物的酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时甲原子得电子数目比乙的多;⑤甲的单质熔沸点比乙的低.能说明甲比乙的非金属性强的是( )
A.①②③
B.只有⑤
C.只有④
D.①②③④⑤
参考答案:①甲比乙容易与H2化合,可说明甲比乙的非金属性强,故①正确;
②甲的氢化物比乙的氢化物稳定,可说明甲比乙的非金属性强,故②正确;
③甲的最高价氧化物对应的水化物的酸性比乙的最高价氧化物对应的水化物酸性强,可说明可说明甲比乙的非金属性强,故③正确;
④与某金属反应时甲原子得电子数目比乙的多,不能说明可说明甲比乙的非金属性强,非金属性的强弱只与等电子的能力有关,故④错误;
⑤甲的单质熔沸点比乙的低,属于物理性质,与得失电子的能力无关,不能用来判断非金属性的强弱,故⑤错误.
正确的有①②③,
故选A.
本题解析:
本题难度:一般