1��ʵ���� ��10�֣�Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч����������ͬѧ�ֱ��������ͼһ��ͼ����ʾ��ʵ�顣
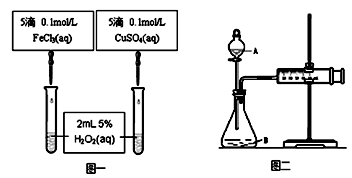
��1��ͼһ��ͨ���۲�_____________________________ ���������ԱȽϵó����ۡ���ͬѧ�����CuSO4��ΪCuCl2��Ϊ��������������__________________________��
����Ϊ���������������ָĽ��� _____________________________________________��
��2��ͼ�������ڶ����ȽϷ�Ӧ�Ŀ��������ͼ��װ�������Եķ����� ��
����ͼ����ʵ��ʱ������������� ��
�ο��𰸣���10�֣�(ÿ��2��)
��1����Ӧ�������ݿ�������Ӧ��ɵ��Ⱥ���Թܱڵ����ȳ̶ȣ� ��2�֣�
������������ͬ���ų������ӵĸ��ţ�2�֣�
��FeCl3��ΪFe2(SO4)3 ��2�֣�
��2���ر�A����������ע������������һ�����룬һ��ʱ����ɿ��������۲�����Ƿ�ص�ԭλ����ص�ԭλ֤�����������á���2�֣�
һ��ʱ�����ռ���������������ռ�һ���������������Ҫ��ʱ�䣨2�֣�
���������(1���Ƚ����κ�ͭ�ζ�H2O2�ֽ�Ĵ�Ч�������ǹ۲�������ݵĿ���������ͭ���Ȼ�����������Ӳ�ͬ������Ӱ��ʵ�������ʽ�������Ӹij���ͬ�ģ������ų������ʵ������Ӱ�죬
��2����װ���л����ǻ�ģ���ͨ�����������������ı�װ���ڲ���ѹǿ��ǰ��ر�A��������
�÷�Ӧ��ͨ����������ķ�Ӧ���ʷ����жϵģ����Ը���v=��V/��t����֪����Ҫ�����������Dz���40ml��������Ҫ��ʱ��
�����Ѷȣ�һ��
2������� ��ӦA(g)+B(s)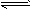 C(g)����H��0����������������ʱ���ı�����һ��������������C�����ʣ�
C(g)����H��0����������������ʱ���ı�����һ��������������C�����ʣ�
��1������_______��
��2������ѹǿ________ ��
��3�����������ݻ�________ ��
��4������A_______��
��5������B________��?
��6����������________��
�ο��𰸣���1���ӿ�
��2���ӿ�
��3������
��4���ӿ�
��5������
��6���ӿ�
���������
�����Ѷȣ�һ��
3��ʵ���� H2O2��ʵ���ҳ��õ�һ�ֻ�ѧ�Լ���ijʵ��С����H2O2�ֽ�Ϊ�����о�Ũ�ȡ���������Һ����ԶԷ�Ӧ���ʵ�Ӱ�졣�ڳ����°������·������ʵ�顣
ʵ����
| ��Ӧ��
| ����
|
��
| 10mL2% H2O2��Һ
| ��
|
��
| 10mL5% H2O2��Һ
| ��
|
��
| 10mL5% H2O2��Һ
| 1mL0��1mol��L-1FeCl3��Һ
|
��
| 10mL5% H2O2��Һ+����HCl��Һ
| 1mL0��1mol��L-1FeCl3��Һ
|
��
| 10mL5% H2O2��Һ+����NaOH��Һ
| 1mL0��1mol��L-1FeCl3��Һ
|
��1��ʵ��ٺ͢ڵ�Ŀ����_ ������ ������
��2��ʵ��ۡ��ܡ����У�������������������ʱ��仯�Ĺ�ϵ����ͼ��������ͼ�ܹ��ó��Ľ����� ��
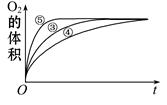
��3��Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч����ij��ѧ�о�С���ͬѧ���������ͼ��ʾ��ʵ��װ�ý���ʵ�顣
ʵ��ʱ��������40mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԣ���ʵ������Ҫ���������� ��
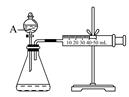
��4��H2O2������H2SO4 �ữ��FeSO4,���ӷ���ʽΪ ��
�ο��𰸣���8�֣���1��̽��H2O2��Һ��Ũ�ȵı仯�Էֽ����ʵ�Ӱ�졣
��2��ͼ����ʾFeCl3��Һ�Ĵ����ã�����������Ч���Ϻã�����������Ч��������
��3���������ֱ���Fe3+��Cu2+�Ĵ������£��ռ�40mL�����ʼ����ʱ�䣬���ܼ������Ӧ���ʡ�
��4��Fe2++2H2O2+4H+�� Fe3++4H2O
�����������1�����ݱ������ݿ�֪��ʵ��٢��в�֮ͬ������˫��ˮ��Ũ�Ȳ�ͬ������ʵ��Ŀ����̽��H2O2��Һ��Ũ�ȵı仯�Էֽ����ʵ�Ӱ�졣
��2����ͼ��֪���ݵķ�Ӧ������ܵķ�Ӧ������С�����ʵ�鷽����֪�����Ի���������H2O2�ֽ�����ʣ����Ի����ܼ�СH2O2�ֽ�����ʣ���ʵ�������ͼ����ʾFeCl3��Һ�Ĵ����ã�����������Ч���Ϻã�����������Ч��������
��3��Ҫ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч����Ӧ����ͬ������������һ���������Ƚϣ�ͬʱ����Ҫ�����������ֱ���Fe3+��Cu2+�Ĵ������£��ռ�40mL�����ʼ����ʱ�䣬���ܼ������Ӧ���ʡ�
��4��˫��ˮ���������ԣ��ܰ����������������������ӣ���Ӧ�����ӷ���ʽ��Fe2++2H2O2+4H+��Fe3++4H2O��
���㣺����Ӱ�컯ѧ��Ӧ�������ص�ʵ��̽��
��������������е��Ѷȵ����⣬�����ۺ���ǿ�����ض�ѧ��ʵ��̽�������������������ڼ���ѧ����ѧϰ�����ԣ�Ҳ����������ѧ���Ĺ淶ʵ��������������Ը���������Ҫ����ʵ���������Ϊ���ģ�ͨ����ʲô��Ϊʲô���������ص㿼��ʵ����������Ĺ淶�Ժ�ȷ�Լ��������֪ʶ���ʵ������������������ܽϺõĿ���ѧ��ʵ����ơ����ݴ�����ͼ��������ۺ��������ڽ��ʱע����֪��Ϣ�����á�
�����Ѷȣ�����
4������� ijѧ����0��1��10��25�L3������������99��5%����Ƭ���ᷴӦ��ȡH2��ʵ��������±�

��1��д����Ƭ���ᷴӦ�����ӷ���ʽ________________________��
��2����Ӧ1-15min�ڣ���������ķ�Ӧ�����ӿ죬��ԭ����_____________________________��
��3��������Ƭ����������ᷴӦ����IJ��죬����˼�������������²��룺
����һ��____________________________________��
�������____________________________________��
�ο��𰸣���1��2Al+6H+==2Al3++3H2��
��2����Ӧ�����¶����ߣ���ѧ��Ӧ���ʼӿ�
��3������һ��Cl-�Ը÷�Ӧ�дٽ�����
�������SO42-�Ը÷�Ӧ����������
���������
�����Ѷȣ�һ��
5��ѡ���� Ϊ����ȡ�⣬��ͨ����Ӧ��2NO+O2==2NO2?NO2+2H+ +2I- ="=NO" + I2+H2O�Ƶã�NO���Ƶ�����е�������
A����ԭ��
B��������
C������
D����Ӧ��
�ο��𰸣�C
������������ݷ�Ӧ�۲��֪��Ӧǰ��NO�ĵ�����û�з����仯���������˻�ѧ��Ӧ��������������ã�����C��
�����Ѷȣ���