1、选择题 加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。下列说法正确的是
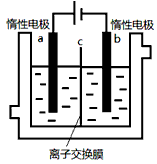
[? ]
A.a电极是阴极
B.a极区的KI最终转变为KIO3
C.阳极电极反应:4OH--4e-==2H2O+O2↑
D.电解过程中OH-从a极区通过离子交换膜c进入b极区
参考答案:B
本题解析:
本题难度:一般
2、选择题 已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8的含有 Fe2(SO4)3杂质的CuSO4溶液中加入适量的黑色粉末X,充分搅拌后过滤,将滤液用如图所示装置电解,其中某电极增重ag,另一电极上产生标准状况下的气体y mL。
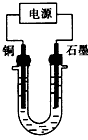
下列说法正确的是
[? ]
A.黑色粉末X是铁粉
B.铜电极连接电源正极
C.石墨电极上发生的反应是4OH--4e-=O2↑+2H2O
D.铜的相对原子质量的计算式是
参考答案:C
本题解析:
本题难度:一般
3、选择题 有三个烧杯,分别盛有CuCl2、KCl和AgNO3三种溶液,均以Pt作电极,将它们串联在一起电解一定时间,测得电极增重总和2.8克,这时产生的有色气体与无色气体的物质的量之比为(? )
A.4∶1
B.1∶1
C.4∶3
D.3∶4
参考答案:C
本题解析:串联电路中,相同时间内各电极得失电子的物质的量相同,各电极上放出气体的物质的量之比为定值。不必注意电极增重是多少,只要判断出生成何种气体及生成该气体一定物质的量所得失电子的物质的量,就可以通过电子守恒,判断气体体积之比。第一只烧杯中放出Cl2,第二只烧杯中放出Cl2和H2,第三只烧杯中放出O2。在有1mol电子转移下,分别是0.5mol、0.5mol、0.5mol和0.25mol。所以共放出有色气体0.5mol+0.5mol=1mol,无色气体0.5mol+0.25mol=0.75mol。
本题难度:一般
4、填空题 某课外活动小组设计了如图所示的装置,调节滑动变阻器,控制电流强度适中的情况下用其进行缓慢电解NaCl溶液及相关实验(此时,打开止水夹a,关闭止水夹b)。由于粗心,实验并未达到预期目的,但也看到了令人很高兴的现象(阳离子交换膜只允许阳离子和水的通过)。请帮助他们分析并回答下列问题:
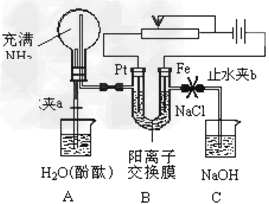
(1)写出B装置中的电极反应:阴极:____________?阳极:____________? ?
(2)回答观察到A装置中的现象: ①_________; ②烧瓶中液面上升到高于左侧尖嘴一定程度后又逐渐下落至与尖嘴相平; ③________?。
(3)当观察到A装置中的现象后,他们关闭止水夹a,打开止水夹b。再观察C装置,若无现象,说明理由,若有现象,请写出有关反应的化学方程式(是离子反应的写离子方程式):___________?
(4)若想达到电解NaCl溶液的目的,应如何改进装置,请提出你的意见。 ______________。
参考答案:(1)2H2O+2e-==2OH-+?H2↑(或2H+?+?2e-==H2↑)?;Fe-2e-==?Fe2+?
(2)①A烧杯中的H2O倒吸并产生红色喷泉?
③最后A烧杯溶液呈红色,导管有气泡溢出?
(3)?Fe2+?+2OH-==?Fe(OH)2↓;4Fe(OH)2?+?2H2O?+?O2==?4Fe(OH)3 ?(或4Fe2+?+?8OH-+?2H2O?+?O2==?4Fe(OH)3↓)?
(4)把Fe电极换成C、Pt等惰性电极或将装置中两电极调换位置等
本题解析:
本题难度:一般
5、填空题 (18分)(Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题:
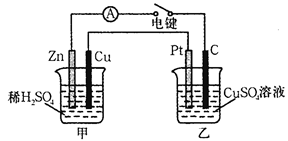
(1)甲装置的名称是_____(填“原电池”或“电解池”)。
(2)写出电极反应式:Pt极 ;
当甲中产生0.1 mol气体时,乙中析出铜的质量应为___________。
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色_______(填“变深”、“变浅”或“无变化”)。
(4)若乙池溶液通电一段时间后,向所得的溶液中加入0.1mol的Cu(OH)2后恰好恢复到电解前的浓度。则电解过程中转移电子的数目为 。(用NA表示)
(Ⅱ)由Cu2+、Cl-、Na+、SO42-四种离子中的两种离子组成的电解质溶液若干种,可选用铁电极、铜电极、铂电极进行电解实验。
(1)欲使铁制品表面镀铜,应以_______为阳极,电解质溶液为 。
(2)以铂作阳极电解 溶液时,溶液的碱性有明显增强,且溶液保澄清,电解时总反应的化学方程式为 。
参考答案:Ⅰ.(1)原电池;(2)2Cl--2e-=Cl2↑、 6.4g;(3) 变深 ;(4) 0.4NA;
Ⅱ.(1) 铜 、硫酸铜或氯化铜溶液 ;(2) 氯化钠溶液
本题解析:(Ⅰ)(1)根据图中的铜、锌两种电极和电解质稀硫酸构成闭合电路知:该装置为原电池,Zn活泼,则Zn作负极,Cu作正极,发生电池反应为Zn+H2SO4
本题难度:一般