| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《电解池原理》在线测试(2019年最新版)(四)
参考答案:D 本题解析:A、将Cu投入稀硫酸中,铜和稀硫酸不反应,A错误;B、让Cu在潮湿的环境发生电化学腐蚀,发生的应该是吸氧腐蚀,B错误;C、将Cu投入浓硫酸中并加热生成SO2,C错误;D、用Cu作电极、稀硫酸作电解质溶液电解,铜是阳极失去电子,阴极氢离子发生生成氢气,D正确,答案选D。 本题难度:一般 3、选择题 已知电解(石墨电极)盐酸、硫酸混合酸时两极生成的气体与时间关系如图所示。则其电解过程中溶液pH随时间变化关系的正确图形是下列的 参考答案:B 本题解析: 本题难度:一般 4、简答题 用石墨电极电解500mL饱和食盐水,通电一定时间后,在一个电极上收集到标准状况下1.12L氯气. 参考答案:(1)用石墨电极电解500mL饱和食盐水,阳极电极上收集到标准状况下1.12L氯气,物质的量为0.05mol,另一电极是氢离子得到电子生成氢气,电极反应为 2H++2e-=H2↑,依据电子守恒计算得到,Cl2~2e-~H2,生成氢气物质的量为0.05mol,质量为0.05mol×2g/mol=0.1g; 本题解析: 本题难度:一般 5、选择题 将1L含有0.4molCuSO4和0.2molNaCl的水溶液用惰性电极电解,电解一段时间后,在一个电极上增重19.2 g,另一个电极上产生气体(标况)的体积是 |
参考答案:A
本题解析:在一个电极上增重19.2 g的铜,则转移电子0.6mol,另一电极先后发生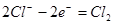 、
、 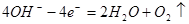 ,转移电子0.6mol,生成氢气0.1mol,生成氧气0.1mol,另一个电极上产生气体(标况)的体积是4.48L。
,转移电子0.6mol,生成氢气0.1mol,生成氧气0.1mol,另一个电极上产生气体(标况)的体积是4.48L。
考点:本题考查电化学计算。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《键参数――.. | |