1、选择题 对100mL 1mol・L-1的Na2CO3溶液,下列说法不正确的是
A.将溶液稀释,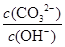 减少
减少
B.滴人含0.l mol CH3COOH的溶液:c ( CH3 COO一)<c( HCO3一)
C.通人0.1 mo1CO2气体,溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3)
D.滴人酚酞,微热,溶液颜色加深
参考答案:B
本题解析:A、碳酸钠溶液中CO32-水解,稀释促进水解,因此CO32-的物质的量减少和OH-的物质的量增加,所以将溶液稀释,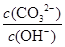 减少,A正确;B、滴人含0.l mol CH3COOH的溶液中二者反应恰好生成碳酸氢钠和醋酸钠,由于醋酸的酸性强于碳酸的,因此醋酸钠的水解程度小于碳酸氢钠的水解程度,所以溶液中c ( CH3 COO一)>c( HCO3一),B不正确;C、通人0.1 mo1CO2气体,二者恰好反应生成碳酸氢钠,根据物料守恒可知溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3),C正确;D、水解吸热,滴人酚酞,微热,促进水解,溶液碱性增强,因此溶液颜色加深,D正确,答案选B。
减少,A正确;B、滴人含0.l mol CH3COOH的溶液中二者反应恰好生成碳酸氢钠和醋酸钠,由于醋酸的酸性强于碳酸的,因此醋酸钠的水解程度小于碳酸氢钠的水解程度,所以溶液中c ( CH3 COO一)>c( HCO3一),B不正确;C、通人0.1 mo1CO2气体,二者恰好反应生成碳酸氢钠,根据物料守恒可知溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3),C正确;D、水解吸热,滴人酚酞,微热,促进水解,溶液碱性增强,因此溶液颜色加深,D正确,答案选B。
本题难度:一般
2、选择题 对于等物质的量浓度的Na2CO3和NaHCO3溶液,下列说法不正确的是(? )
A.分别升高温度,两种溶液的pH均减小
B.相同温度下两种溶液的pH:Na2CO3> NaHCO3
C.分别加入少量NaOH,两溶液中c(CO32-)均增大
D.两溶液均存在c(Na+) + c(H+)=c(OH-) + c(HCO3-) + 2c(CO32-)
参考答案:A
本题解析:Na2CO3和NaHCO3溶液均水解呈碱性,升高温度水解程度增大,pH增大,A错误;越弱越水解,等浓度时Na2CO3 水解强于NaHCO3溶液,所以B正确;加入NaOH,c(OH-)增大,使Na2CO3 水解平衡左移,c(CO32-)增大,而NaHCO3溶液与NaOH反应生成Na2CO3 ,所以c(CO32-)也增大,C正确;两溶液中存在的离子相同,所以满足电荷守恒c(Na+) + c(H+)=c(OH-) + c(HCO3-) + 2c(CO32-),D正确;故选A。
本题难度:一般
3、填空题 (4分)盐碱地(含较多NaCl、Na2CO3)不利于作物生长,通过施加适量石膏可以降低土壤的碱性。试用化学方程式分别表示盐碱地产生碱性的原因:?,及用石膏降低其碱性的反应原理:?。
参考答案:(4分) Na2CO3 + H2O= NaOH+NaHCO3?Na2CO3 +CaSO4= Na2SO4+CaCO3↓
本题解析:碳酸钠是强碱弱酸盐,溶于水水解显碱性,水解方程式是Na2CO3 + H2O= NaOH+NaHCO3;石膏是硫酸钙,能和碳酸钠反应生成难溶性的碳酸钙沉淀,从而抑制水解,反应的化学方程式是Na2CO3 +CaSO4= Na2SO4+CaCO3↓。
点评:本题关键是要从平衡的角度去理解如何降低溶液的酸碱性,因此要利用勒夏特例原理。
本题难度:简单
4、选择题
A.焊接时用 NH4C1 溶液除锈
B.使用泡沫灭火器时,使硫酸铝与饱和小苏打溶液混合
C.饱和氯化铁溶液滴入沸水制备 Fe(OH)3胶体
D.生活中用电解食盐水的方法制取消毒液
参考答案:D
本题解析:本题考查盐的水解的应用。盐的水解应用很多, A、B、C项均正确;D是电解后生成的氯气与Na O H反应生成次氯酸盐的缘故,与水解无关,选D。
本题难度:一般
5、选择题 下列叙述正确的是(?)
A.在0.1mol・L-1CH3COONa溶液中,c (OH-)==c(CH3COOH)+c(H+)
B.10 mL 0.02mol・L-1HCl溶液与10 mL 0.02mol・L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=10
C.0.1mol・L-1氨水中,c(OH-)==c(NH4+)
D.0.1mol・L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)==2c(A2-)+c(HA-)+c(H2A)
参考答案:A
本题解析:略
本题难度:一般