1��ѡ���� �����������ε�ϡ��Һ���ֱ���a mol��L��1?NaX��Һ��b mol��L��1?NaY��Һ������˵������ȷ����
A����a��b��pH(NaX)��pH(NaY)������ͬŨ��ʱ������HX��HY
B����a��b�������c(X��)��c(Y��)��c(HY) ������ͬŨ��ʱ������HX��HY
C����a��b�����c(X��)��c(Y��)������Ƴ���Һ��c(HX)��c(HY)������ͬŨ��ʱ������HX��HY
D��������Һ�������ϣ����c(X��)��c(Y��)��c(HX)��c(HY)��0.1 mol��L��1������Ƴ�a+b��0.2 mol��L��1 ����������Һ���ʱ��Һ����ĸı䣩
�ο��𰸣�
���������Aѡ����������ҺŨ����ͬ��PH��NaX��> PH��NaY��,NaX�ļ��Ը�ǿ����Ӧ��X-��ˮ��̶ȸ�ǿ���������HX<HY��Bѡ����a��b����c(X��)��c(Y��)��c(HY)����˿��Կ���X-û��ˮ�⣬���Ϊǿ�ᣬ������HX��HY��Cѡ����a��b����c(X��)��c(Y��)�����Ե�֪X-ˮ��IJ��ִ���Y��ˮ��IJ��֣�����c(HX)��c(HY)������ͬŨ��ʱ������HX��HY��Dѡ�������������ϣ����Ϻ������ǻ��ǰ������������c(X��)��c(Y��)��c(HX)��c(HY)=��a+b��/2,����Ϊc(X��)��c(Y��)��c(HX)��c(HY)��0.1mol/L�����Եõ�a+b��0.2mol/L��
���������⽫����ˮ��Ļ���֪ʶ������ۺϿ��죬������Ҫ��Ƚϸߣ�����һ���Ѷ���Ŀ��
�����Ѷȣ�һ��
2��ѡ���� ��������0.10 mol /L KOH��Һ���ζ�0.10 mol /L CH3COOH��Һ���йصζ������е�˵����ȷ����
A���ζ��յ�ʱ����Һ��pH=7
B���ζ��յ�ʱ��c(K+) = c(CH3COO�� )��c(H+) < c(OH��)
)��c(H+) < c(OH��)
C������ҺpH=7ʱ��c(K+) =  c(CH3COO��) + c
c(CH3COO��) + c (CH3COOH)
(CH3COOH)
D���ӽ��ζ��յ�ʱ��c(K+) + c(H+) = c(CH3COO��) + c(OH��)
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
3��ѡ���� ��0.1mol/L��Na2CO3����Һ�У����й�ϵʽ��ȷ����
A��c(Na+)>c(CO32-)> c(OH��)> c(H+)
B��c(OH��)= c(HCO3��)+ c(H2CO3)
C��2c(Na+)=c(CO32-)+ c(HCO3��)> c(H2CO3)
D��c(Na+)+ c(H+)= c(OH��) + c(HCO3��) +2c(CO32-)
�ο��𰸣�AD
���������A��CO32?ˮ��ʹ��Һ�ʼ��ԣ�����c(Na+)>c(CO32-)> c(OH��)> c(H+)����ȷ��B�����������غ�ɵã�c(OH��)= c(HCO3��)+ 2c(H2CO3)+c(H+)������C�����������غ�ɵ�c(Na+)="2" c(CO32-)+ 2c(HCO3��)+2 c(H2CO3)������D�����ݵ���غ�ɵã�c(Na+)+ c(H+)= c(OH��) + c(HCO3��) +2c(CO32-)����ȷ��
�����Ѷȣ�һ��
4��ѡ���� һ������(NH4)2SO4��NH3��H2O������õļ�����Һ�У�����˵���������
A��c(OH�C) > c(H+)
B��c(NH4+) + c(H+) = 2c(SO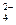 )+ c(OH�C)
)+ c(OH�C)
C��c(NH4+)<2c(SO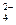 )
)
D��c(NH4+)> 2c(SO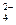 )
)
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
5������� ��Ԫ�صĺ��������ڹ�ҵ����;�㷺�����������ա�
��ҵ����Na2SO3��Һ������ҵβ���е�SO2���±����ݱ�ʾ��Ӧ������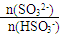 ��pH�仯�Ĺ�ϵ��
��pH�仯�Ĺ�ϵ��
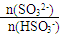
| 91:9
| 1:1
| 9:91
|
������pH
| 8.2
| 7.2
| 6.2
|
?
��1������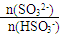 = 1ʱ����ҺpH= 7.2��ԭ��___________________������0.20 mol/L ��NaOH��Һ����Ӧǰ����Һ������䣩����SO2������Ӧ����Һ�����ԣ���
= 1ʱ����ҺpH= 7.2��ԭ��___________________������0.20 mol/L ��NaOH��Һ����Ӧǰ����Һ������䣩����SO2������Ӧ����Һ�����ԣ���
c (HSO3-) + 2c (SO32-) =" _______" mol/L ��
��2����֪��Ki1(H2SO3)> Ki(HAc) > Ki2(H2SO3) > Ki2(H2CO3)��ҪʹNaHSO3��Һ��c(Na+):c(HSO3-)�ӽ�1:1��������Һ�м�������____________��
a��H2SO3��Һ? b��NaOH��Һ? c��������? d��Na2CO3
��3��ʵ����ͨ�����µ��KHSO4��Һ�Ʊ����������K2S2O8��д������KHSO4�ĵ��뷽��ʽ��__________________________________________��
��4��S2O82-��ǿ�����ԣ���ԭ����ΪSO42-�������̣�MnSO4��������أ�K2S2O8����������Һ�������Ӵ��¿ɷ�����Ӧ���õ��Ϻ�ɫ��Һ����д�˷�Ӧ�Ļ�ѧ����ʽ��??��
��5����֪��S2O32-�н�ǿ�Ļ�ԭ�ԣ�ʵ���ҿ���I-�ⶨK2S2O8��Ʒ�Ĵ��ȣ���Ӧ����ʽΪ��
S2O82-��2I-��2SO42-��I2 ������? I2��2S2O32-��2I-��S4O62-������
S2O82-��S4O62-��I2������ǿ��˳��__________________________��
��6��K2S2O8��ƫ����ϩ��CH2=CF2���ۺϵ���������ƫ����ϩ��CH3��CClF2������ȥHCl�Ƶã�����0.5 molƫ����ϩ����Ҫ����54 kJ���ȣ�д����Ӧ���Ȼ�ѧ����ʽ_______��
�ο��𰸣���1��HSO3-�ĵ���̶���SO32-��ˮ��̶������1�֣�? 0.2 mol/L��2�֣�
��2��a c��2�֣�
��3��KHSO4 ��K+ + HSO4-?��1�֣�
��4��5K2S2O8?+ 2MnSO4 ?+ 8H2O�� 4K2SO4 + 2KMnO4 + 8H2SO4��2�֣�
��5��S2O82- > I2 > S4O62-?��2�֣�?
��6��CH3��CClF2(g) �� CH2=CF2(g) + HCl(g)�C108kJ��2�֣�
�����������1������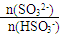 = 1ʱ����ҺpH= 7.2��ԭ��HSO3-�ĵ���̶���SO32-��ˮ��̶��������ʱ��Һ�ӽ����ԣ����ݵ���غ㣬����0.20 mol/L ��NaOH��Һ����Ӧǰ����Һ������䣩����SO2������Ӧ����Һ�����ԣ���c (HSO3-) + 2c (SO32-) ="c" (Na+)= 0.2 mol/Lmol/L ��
= 1ʱ����ҺpH= 7.2��ԭ��HSO3-�ĵ���̶���SO32-��ˮ��̶��������ʱ��Һ�ӽ����ԣ����ݵ���غ㣬����0.20 mol/L ��NaOH��Һ����Ӧǰ����Һ������䣩����SO2������Ӧ����Һ�����ԣ���c (HSO3-) + 2c (SO32-) ="c" (Na+)= 0.2 mol/Lmol/L ��
��2����֪��Ki1(H2SO3)> Ki(HAc) > Ki2(H2SO3) > Ki2(H2CO3)��ҪʹNaHSO3��Һ��c(Na+):c(HSO3-)�ӽ�1:1������Ϣ�п��Կ������������������̶ȴ�����ˮ��̶ȣ���ֻҪ��������뼴�ɣ�������Һ�м�������a��H2SO3��Һ��c�������ᡣ
��3��KHSO4����������Ӻ��������������KHSO4�ĵ��뷽��ʽKHSO4 ��K+ + HSO4- ��
��4���õ��Ϻ�ɫ��ҺӦ���Ǹ�����أ��ٸ���������ԭԭ����д�˷�Ӧ�Ļ�ѧ����ʽΪ5K2S2O8?+ 2MnSO4 ?+ 8H2O�� 4K2SO4 + 2KMnO4 + 8H2SO4��
��5�������������������Դ�����������������Թ��ɣ����Ʋ�ΪS2O82-��2I-��2SO42-��I2 �����٣��ɵó� S2O82- > I2����ͨ����Ӧ I2��2S2O32-��2I-��S4O62-�����ڿɵó� I2 > S4O62- ���� S2O82-��S4O62-��I2������ǿ��˳��S2O82- > I2 > S4O62- ��
��6�������Ȼ�ѧ����ʽ����д������д��CH3��CClF2(g) �� CH2=CF2(g) + HCl(g)�C108kJ��
�����Ѷȣ�һ��